时间:2017-09-23 23:58:36
1、选择题 下列反应对应的离子方程式书写正确的是(?)。
A.漂白粉露置在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
B.氢氧化钡溶液与硫酸氢钠溶液反应后溶液恰好为中性:Ba2++H++SO42-+OH-=BaSO4↓+H2O
C.Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑
D.在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:4OH-+3ClO来源:91考试网 www.91eXam.org-+2Fe(OH)3=2FeO42-+3Cl-+5H2O
参考答案:D
本题解析:本题考查离子方程式的正误判断,意在考查考生规范书写化学用语的能力。A项,漂白粉变质生成碳酸钙,不可能生成碳酸氢钙,其离子方程式为Ca2++2ClO+CO2+H2O=CaCO3↓+2HClO;B项,氢氧化钡溶液与硫酸氢钠溶液反应后溶液恰好为中性,正确的离子反应方程式是Ba2++2H++SO42-+2OH-=BaSO4↓+2H2O;C项,正确的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑。
本题难度:一般
2、选择题 下列离子方程式表达正确的是
[? ]
A.用惰性电极电解氯化镁溶液:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.碳酸氢钠溶液与过量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
C.NaHSO4溶液中滴入Ba(OH)2溶液至SO42-完全沉淀:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
D.向明矾溶液中滴加过量氨水:Al3++4NH3・H2O=AlO2-+4NH4++2H2O
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列说法正确的是( )
A.由于水分子之间存在氢键,所以水分子比较稳定
B.晶体中有阴离子则必然有阳离子,有阳离子一定有阴离子
C.NH4HSO3溶液与足量NaOH溶液混合加热:NH4++HSO3-+2OH-
? |
参考答案:A.由于水分子之间存在氢键,则水的沸点高,其稳定性与化学键有关,与氢键无关,故A错误;
B.金属晶体中有阳离子,但没有阴离子,而离子晶体中有阳离子也有阴离子,故B错误;
C.NH4HSO3溶液与足量NaOH溶液混合加热,反应生成亚硫酸钠、水、氨气,则离子反应为NH4++HSO3-+2OH-?△?.?NH3↑+SO32-+2H2O,故C正确;
D.水为极弱电解质,可加硫酸增强导电性,但不能加盐酸,若加盐酸,电解生成氢气和氯气,故D错误;
故选C.
本题解析:
本题难度:简单
4、选择题 下列化学反应,能用离子方程式CO32-+2H+= CO2↑+H2O来表示的是
[? ]
参考答案:B
本题解析:
本题难度:简单
5、填空题 (16分)实验室中以粗铜(含杂质)为原料,某种制备铜的氯化物的流程如下:
按要求回答下列问题:
(1)操作①的所用到的玻璃仪器有______________。
(2)上述流程中,所得固体1需要加稀盐酸溶解,其理由是?;
溶液1可加试剂X用于调节pH以除去杂质,?X可选用下列试剂中的(填序号)___________。
A.NaOH?B.NH3・H2O? C.CuO? D.CuSO4?
(3)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出?
制备CuCl的离子方程式:?。
(4)现用如图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。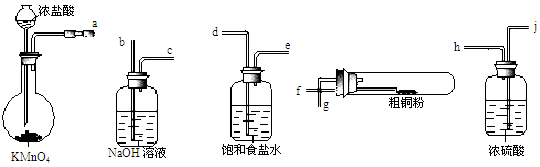
①按气流方向连接各仪器接口顺序是:a→?、 → 、 → 、 → 。实验中大试管加热前要进行一步重要操作,其操作是?。
②反应时,盛粗铜粉的试管中的现象是?。
(5)在溶液2转化为CuCl2・2H2O的操作过程中,发现溶液颜色由蓝色变为绿色。小组同学欲探究其原因。已知:氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) + 4Cl-(aq)? ?CuCl42-(aq) + 4 H2O (l)
?CuCl42-(aq) + 4 H2O (l)
蓝色?绿色
该同学取氯化铜晶体配成蓝绿色溶液Y,进行如下实验,其中能证明溶液中有上述转化关系的是?(填序号)。
A.将Y稀释,发现溶液呈蓝色?B.在Y中加入CuCl2晶体,溶液变为绿色
C.在Y中加入NaCl固体,溶液变为绿色?D.取Y进行电解,溶液颜色最终消失
参考答案:(1)漏斗、烧杯、玻璃棒;(2)抑制氯化铜、氯化铁水解;C D;
(3)SO2+2H2O+2Cu2++2Cl-=2CuCl+SO42-+4H+;
(4)①dehifgb;通入一段时间的氯气,将装置中的空气排尽;②产生大量棕黄色的烟;(5)ABC
本题解析:(1)操作①是过滤。所用到的玻璃仪器有漏斗、烧杯、玻璃棒;(2)Cu与Cl2反应得到CuCl2,杂质也与氯气反应得到金属氯化物。CuCl2是强酸弱碱盐,容易水解,为了抑制氯化铜、氯化铁水解溶解固体在稀盐酸的环境中。溶液1的主要成分是CuCl2,若加试剂X用于调节pH以除去杂质,?X应该是含有Cu2+的物质。选项为CD。(3)根据题意结合电子守恒、电荷守恒及原子守恒可得方程式:SO2+2H2O+2Cu2++2Cl-=2CuCl+SO42-+4H+;(4)①要经过制取气体、除去杂质、气体干燥、发生反应、尾气处理等实验步骤。按气流方向连接各仪器接口顺序是:a→d→e→h→i→f→g→b。实验中大试管加热前要进行一步重要操作,其操作是通入一段时间的氯气,将装置中的空气排尽再进行实验,否则Cu会被氧化为CuO;②在大试管发生反应:Cu+ Cl2 CuCl2,盛粗铜粉的试管中的现象是产生大量棕黄色的烟;(5)A.将Y稀释,即加入水,若存在上述平衡,则增大了水的浓度,平衡逆向移动,产生更多的蓝色的Cu(H2O)42+(aq)。正确。?B.在Y中加入CuCl2晶体,即增大了c(Cl-)的浓度,平衡正向移动,绿色的CuCl42-(aq)的浓度增大。溶液变为绿色。正确。C.在Y中加入NaCl固体,c(Cl-)的浓度增大,平衡正向移动,绿色的CuCl42-(aq)的浓度增大,溶液变为绿色。正确。D.取Y进行电解,溶液颜色最终消失,这与是哪种结合方式无关。错误。
CuCl2,盛粗铜粉的试管中的现象是产生大量棕黄色的烟;(5)A.将Y稀释,即加入水,若存在上述平衡,则增大了水的浓度,平衡逆向移动,产生更多的蓝色的Cu(H2O)42+(aq)。正确。?B.在Y中加入CuCl2晶体,即增大了c(Cl-)的浓度,平衡正向移动,绿色的CuCl42-(aq)的浓度增大。溶液变为绿色。正确。C.在Y中加入NaCl固体,c(Cl-)的浓度增大,平衡正向移动,绿色的CuCl42-(aq)的浓度增大,溶液变为绿色。正确。D.取Y进行电解,溶液颜色最终消失,这与是哪种结合方式无关。错误。
本题难度:一般