时间:2017-09-23 23:43:29
1、推断题 工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下: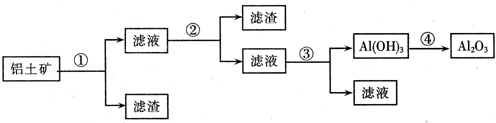
(可供选择的试剂:稀盐酸、NaOH溶液、稀氨水,CO2等)
请写出你所设计的方案中以下各步反应涉及的化学方程式.
①____________________________________________________________________
②____________________________________________________________________
④___________________________________________
2、推断题 物质X、Y、Z有如下转化关系: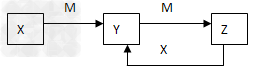
请回答下列问题:
(1)若X、Y、Z中均含有铝元素,则Y的化学式是____________,实验室用明矾制取该物质的离子方程式为___________________。
(2)若M是某元素的最高价氧化物且为气态,此元素的最高价与最低价化合价代数和为0?,X是由电子数均为10的阴阳离子组成,则Y溶液中离子浓度大小的顺序为___________________________。
(3)?若X为黄绿色气体,M是常见金属。完成下列问题:
①?X能与石灰乳反应制取漂白粉,其离子方程式_________________
②含M的一种盐可以作为杀菌消毒、净水剂,其一种制备方法是:以M(OH)3、NaClO和KOH为原料,请写出此反应的离子方程式___________________
③M(OH)3溶液中存在如下的沉淀溶解平衡:M(OH)3(s) M3+?(aq)?+?3OH-(aq)? 常温下,M(OH)3的溶度积Ksp?=?4.0?×?10-38,要使M3+离子浓度降至10-5mol/L,溶液的PH应调至_________。?(lg2=0.3,lg5=0.7)
M3+?(aq)?+?3OH-(aq)? 常温下,M(OH)3的溶度积Ksp?=?4.0?×?10-38,要使M3+离子浓度降至10-5mol/L,溶液的PH应调至_________。?(lg2=0.3,lg5=0.7)
3、选择题 已知,A为空气中含量最多的单质。根据下图转化关系,回答下列问题:
(1)写出下列物质的化学式:
A?、D?。
(2)E→C的反应方程式为?。
(3)久置的E的浓溶液常常呈黄色,原因是?。
(4)实验室制取B的化学方程式为____________________________________。
(5)现有1.00mol・L-1的E溶液,从中取出10.00 mL。此10.00 mL溶液的物质的量浓度为??mol・L-1。将前面取出的E溶液配制成0.100mol・L-1的稀溶液,所需的玻璃仪器除烧杯、玻璃棒外,还需?和??。在配制过程中定容时俯视,则所配溶液浓度??(填“偏大”或“偏小”或“无影响”)。
4、推断题 单质A、B、C和化合物D、E、F,在一定条件下有如下图的转化关系:(有部分反应物或者生成物未标出)
请回答下列问题:
(1)若A是空气的主要成分之一,B在C中燃烧火焰呈苍白色。则C的名称是_______,D与E反应生成F的化学方程式是__________________________________,反应的现象是_______________________。D在催化剂作用下被氧气氧化是工业制备硝酸的主要反应之一,该反应的化学方程式是___________________________________________________。
(2)若A是金属单质,D是淡黄色固体,E是无色无味的液体。则D的用途之一是__________,D与E反应生成F的化学方程式是_____________________________________________。可以通过_________________________实验来检验D中所含的金属元素。
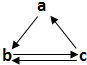
5、选择题 下表所列各物质组中,物质a、b、c之间通过一步反应不能实现如图所示转化的是( )?
| a | b | C A Al2O3 NaAlO2 Al(OH)3 B C CO CO2 C Si SiO2 H2SiO3 D CO2 Na2CO3 NaHCO3 |