时间:2017-09-23 23:00:53
1、选择题 在中和热测定的实验时,应使用的仪器正确组合是( )。
①天平②量筒③烧杯④酒精灯⑤温度计⑥试管⑦量热计⑧环形玻璃搅拌棒
A.①②④⑤⑧ B②③⑤⑦⑧ C. ②③④⑦⑧ D.全部
参考答案:B
本题解析:根据中和热的测定原理可知,在该实验中需要的仪器是选项B。反应不需要称量和加热,所以天平、酒精灯不需要。反应是在烧杯中进行的,不需要试管。答案选B。
本题难度:一般
2、选择题 已知700C时纯水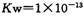 ,下列叙述正确的是
,下列叙述正确的是
A.700C时,向纯水中加人H3PO4后,水的Kw减小
B.700C的Na2CO3溶液中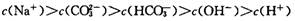
C.700C的H2S04溶液中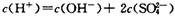
D.将室温下0.1 mol/L的NaOH溶液加热至700C时,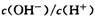 随之增大
随之增大
参考答案:C
本题解析:水的离子积常数只与温度有关,A不正确。碳酸钠水解显碱性,且水解分为两步c(OH-)应大于c(CO32-),B不正确。选项C符合电荷守恒,正确。将0.1 mol/L的NaOH溶液加热至700C时,溶液中的c(OH-)不变,但由于水的离子积常数增大,导致氢离子增大,所以选项D不正确。
本题难度:简单
3、选择题 下列变化中,属于吸热反应的是
A.木炭燃烧反应
B.酸碱中和反应
C.铝和盐酸反应
D.氢氧化钡晶体和氯化铵晶体反应
参考答案:D
本题解析:略
本题难度:简单
4、选择题 25℃时在五份蒸馏水中分别加入适量的下列物质,所得实验结果如下表所示:
| 加入物质 | HCl(aq) | FeCl3 | NaOH | HCOONa | C2H5OH |
| 溶液的pH | 3 | 4 | 10 | 11 | 未测定 |
| 水的电离程度 | α1 | α2 | α3 | α4 | α5 |
参考答案:B
本题解析:略
本题难度:一般
5、选择题 常温下,用0.1000 mol・L-1NaOH溶液滴定20.00 mL 0.1000 mol・L-1CH3COOH溶液所得滴定曲线如下图。下列说法正确的是( )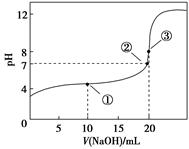
A.点①所示溶液中:
c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:
c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:
c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
参考答案:D
本题解析:由图象知在①点溶液的溶质为CH3COOH与CH3COONa且浓度相同,
由物料守恒得:2c(Na+)=c(CH3COO-)+c(CH3COOH)…①
由电荷守恒得:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)…②
②×2-①得:c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+)
故A错;②点溶液为CH3COONa和CH3COOH的混合溶液且pH=7,V(NaOH)<20 mL,由物料守恒知c(Na+)<c(CH3COOH)+c(CH3COO-);由图象知③点V(NaOH)=20 mL,则溶液为CH3COONa溶液,因为CH3COO-的水解程度很小,所以c(Na+)>c(CH3COO-)>c(OH-)>c(H+);当刚开始滴定时,V(NaOH)很小时,可能有D项不等式成立,所以答案选D。
点评:该题是高考中的常见题型,属于中等难度的试题,试题综合性强,侧重对学生能力的培养,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。
该题的关键是利用好几种守恒关系,即电荷守恒、物料守恒和质子守恒,并能灵活运用即可。
本题难度:简单