时间:2017-09-23 22:53:27
1、选择题 在1molP原子形成的白磷中含有P―P键为(NA为阿氏常数)
A.3NA? B.1.5 NA? C? 4 NA? D 0.25 NA
2、简答题 (1)已知拆开1mol?H-H键、1mol?I-I键、1mol?H-I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由氢气和碘单质反应生成1mol?HI需要?(填“放出”或“吸收”)?kJ的热量.氢气、碘单质和碘化氢三种分子最稳定的是?.
(2)下列五种物质中①Ne?②H2O?③NH3?④KOH?⑤Na2O,只存在共价键的是?,只存在离子键的是?,既存在共价键又存在离子键的是?,不存在化学键的是?.(填写序号)
(3)按要求填空:
①推测Si、N?间氢化物的稳定性;?>?(填化学式)?
②C:?周期?族;
③3416S2-微粒中的质子数是?,中子数是?,核外电子数是?.
(4)对于反应2S02+02
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).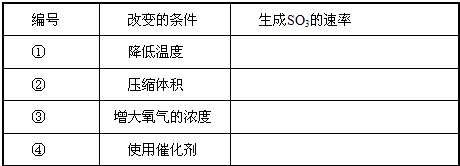
3、选择题 元素X、Y、Z原子序数之和为33,X、Y在同一周期,X+与Z2―具有相同的核外电子层结构。下列推测不正确的是(?)?
A.同周期元素中X的金属性最强
B.同族元素中Z的氢化物沸点最高
C.原子半径X>Y,离子半径X+> Z2―
D.Y的单质和氧化物有相同的晶体类型
4、填空题 (10分)能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的核外电子排布式的简化形式?。
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如右图,分子中碳原子轨道的杂化类型为?;1 mol C60分子中σ键的数目为?。
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓、硫化镉、硫化锌及铜锢硒薄膜电池等。
①第一电离能:As?Se(填“>”、“<”或“=”)。
②二氧化硒分子的空间构型为?。
5、填空题 (12分) 已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下 表。
表。
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数。 |
| Y | 原子核外的L层有3个未成对电子。 |
| Z | 在元素周期表的各元素中电负性仅小于氟。 |
| Q | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
| R | 核电荷数是Y与Q的核电荷数之和 |
| E | 原子序数比R大3 |
 共有?种不同运动状态的电子,有?种不同能级的电子。
共有?种不同运动状态的电子,有?种不同能级的电子。 物中,沸点由高到低
物中,沸点由高到低 的排列次序依次为(写化学式)?。
的排列次序依次为(写化学式)?。 l3? B.[R(H2O)5Cl]Cl2・H2O
l3? B.[R(H2O)5Cl]Cl2・H2O [R(H2O)4Cl2]Cl・2H2O? D.[R(H2O)3Cl3]・3H2O
[R(H2O)4Cl2]Cl・2H2O? D.[R(H2O)3Cl3]・3H2O 污染环境,其反应的化学方程式为??。
污染环境,其反应的化学方程式为??。