ʱ��:2017-09-23 22:32:20
1��ѡ���� �������ʵ��ӻ���ʽ����sp3�ӻ����ǣ����� ��
A��CO2
B��CH4
C��NH3
D��H2O
�ο��𰸣�A��?
�����������������ԭ������ԭ����+����ԭ�ӵŶԵ�����=�ӻ��������CO2��������ԭ��C�ӻ������Ϊ��2+0=2������ȡsp�ӻ���������Ϊsp3�ӻ���
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ���ǣ�������
A���������Ӽ��Ļ�����������ӻ�����
B�����й��ۼ������ʾ��ǹ��ۻ�����
C�����ۻ�������ܺ������Ӽ�
D�����ӻ������в����й��ۼ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3������� ������A�ɶ�����Ԫ��X��Y��ɣ������õ����ȳ�����ϣ���֪��
��1��Ԫ��X��Y��ͬ����?��2��X�ĵ��ʼȿ������ᷴӦ���ֿ���NaOH��Һ��Ӧ��?��3��һ�������£�A��ˮ�����������ɺ�Y�����廯����Z��Z���Ӻ����ĸ�ԭ�Ӻ�10�����ӣ�Z��H2O2��Ӧ�������֮һ��Y�ĵ��ʣ���
��Z��H2O2��Ӧ�Ļ�ѧ����ʽ______��
��X��NaOH��Һ��Ӧ�����ӷ���ʽΪ______��
��A�Ļ�ѧʽ��______��
�ο��𰸣���X�ĵ��ʼȿ������ᷴӦ���ֿ���NaOH��Һ��Ӧ����XΪAl��Ԫ��X��Y��ͬ���ڣ������ڶ�����Ԫ�أ���Y�ڵڶ����ڣ�����һ�������£�A��ˮ�����������ɺ�Y�����廯����Z��Z���Ӻ����ĸ�ԭ�Ӻ�10�����ӣ���YΪN��ZΪNH3��
��XΪAl��YΪN����ZΪNH3��Z��H2O2��Ӧ�������֮һ��Y�ĵ��ʣ���������ԭ��Ӧ��֪��NH3��H2O2��Ӧ����N2��H2O���÷�ӦΪ2NH3+3H2O2�TN2+6H2O��
�ʴ�Ϊ��2NH3+3H2O2�TN2+6H2O��
��Al��NaOH��Һ��Ӧ����ƫ�����ƺ����������ӷ�ӦΪ2Al+2H2O+2OH-�T2AlO2-+3H2�����ʴ�Ϊ��2Al+2H2O+2OH-�T2AlO2-+3H2����
��XΪAl��YΪN��A�ɶ�����Ԫ��X��Y��ɣ���AΪAlN���ʴ�Ϊ��AlN��
���������
�����Ѷȣ�һ��
4������� �±���Ԫ�����ڱ��Ķ����ڲ��֣�������ĸ�ֱ��ʾһ��Ԫ�ء���ش���������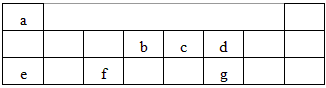
��1��fԪ�������ڱ��е�λ���ǵ�_______���ڵ�________�塣
��2��e��f��Ԫ������������ˮ�������Ӧ�Ļ�ѧ����ʽΪ___________________________
��3��e�ڿ�����ȼ�յIJ���������ѧ��������Ϊ__________��__________��
��4��������ca3�ĵ���ʽΪ____________��c��d����Ԫ���⻯����ȶ��Ը�ǿ����_______�������ʵĻ�ѧʽ����
�ο��𰸣���1��3��IIIA?
��2��NaOH+Al(OH)3==NaAlO2+2H2O?
��3�����Ӽ������ۼ�
��4��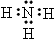 ��H2O
��H2O
���������
�����Ѷȣ�һ��
5��ѡ���� ���������У�ֻ�������Ӽ��Ļ������ǣ�������
A��NaOH
B��MgCl2
C��KBr
D��H2O
�ο��𰸣�BC
���������
�����Ѷȣ���