ʱ��:2017-09-23 22:24:51
1��ѡ���� ��һ����A��Bװ���ݻ�Ϊ1 L�ĺ����ܱ������У�������Ӧ��2A(g)��bB(g)  cC(g)��1 minʱ�ﵽƽ�⣬C��Ũ��Ϊx mol��L��1���������¶Ȳ��䣬���ܱ��������ݻ�ѹ��Ϊԭ����
cC(g)��1 minʱ�ﵽƽ�⣬C��Ũ��Ϊx mol��L��1���������¶Ȳ��䣬���ܱ��������ݻ�ѹ��Ϊԭ����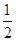 �����´ﵽƽ���C��Ũ��Ϊ2.5 x mol��L��1������˵����ȷ����? (����)
�����´ﵽƽ���C��Ũ��Ϊ2.5 x mol��L��1������˵����ȷ����? (����)
A����ѧ�������Ĺ�ϵ��b<c
B���������ݻ���С�÷�Ӧ���淴Ӧ���ʼ�С
C��ԭ��������B��Ũ�ȱ仯��ʾ�÷�Ӧ��1 min�ڵ�����Ϊ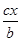 mol��(L��min)��1
mol��(L��min)��1
D���������¶Ⱥ��������ݻ����䣬���뺤��(�����뷴Ӧ)��ƽ�ⲻ�����ƶ�
�ο��𰸣�D
����������������֪��ѹǿ����ƽ��������Ӧ�����ƶ�������b��2>c�����ò���b��c����Դ�С��ϵ��A������������ݻ���С�������淴Ӧ���ʶ�����B�����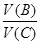 ��
��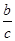 ��v(B)��
��v(B)��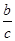 ��v(C)��
��v(C)��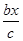 ?mol��(L��min)��1��C�����
?mol��(L��min)��1��C�����
�����Ѷȣ�һ��
2��ѡ���� ��ͼ��ʾ�Ǻ�����ij��ѧ��Ӧ�ķ�Ӧ�����淴Ӧʱ��仯��ʾ��ͼ������������ʾ��ͼ������ϵ���(����)��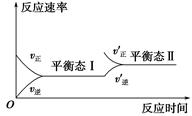
A����Ӧ�ﵽƽ��ʱ������Ӧ���ʺ��淴Ӧ�������
B���÷�Ӧ�ﵽƽ��̬������ӷ�Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��̬��
C���÷�Ӧ�ﵽƽ��̬���С��Ӧ��Ũ�ȣ�ƽ�ⷢ���ƶ����ﵽƽ��̬��
D��ͬһ��Ӧ����ƽ��̬���ƽ��̬��ʱŨ�Ȳ����
�ο��𰸣�C
������������⿼�黯ѧ��Ӧ���ʺͻ�ѧƽ��֪ʶ����ƽ��ʱ�������ʵ�����ʱ��ı仯Ӧ���ٷ����仯������ƽ���ں������ֱ�ߣ���ƽ��̬���Ϊƽ��̬��ͨ������Ӧ��Ũ�ȵķ���ʵ�֡�������ͼ���֪����ƽ�ⷴӦ���ʴ���ԭƽ�ⷴӦ���ʣ����Բ������Ǽ�С��Ӧ���Ũ�ȣ�����C��������ʾ��ͼ������ϡ�
�����Ѷȣ�һ��
3������� (12��)���ŵ���������Ⱦ���������أ��ҹ����ڡ�ʮ���塱�ڼ�Ӵ�Ե��������ŷŵĿ������ȡ�Ŀǰ����������������Ⱦ�ж��ַ�����
��1���û���̿��ԭ��������������йط�ӦΪ��C��g��+2NO(g) N2(g)+CO2(g)?��H.ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO�����£�T1�棩�����·�Ӧ����Ӧ���е���ͬʱ�̲�ø����ʵ�Ũ�����£�
N2(g)+CO2(g)?��H.ij�о�С����ij�ܱ������м���һ�����Ļ���̿��NO�����£�T1�棩�����·�Ӧ����Ӧ���е���ͬʱ�̲�ø����ʵ�Ũ�����£�
| ?Ũ��/mol?L-1 ʱ��/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |

�ο��𰸣���1����0.56?�ڼ���CO2��Ũ�ȣ����������𰸾��ɣ��ۣ�
��2��CH4(g)+2NO2(g)==N2(g)+CO2(g)+2H2O(l)?��H=-955kJ.mol-1
��3��CD? (4)NO2+NO3����e����N2O5
�����������1���ٸ��ݱ������ݿ�֪��ƽ�ⳣ��Ϊ ��
��
�ڸ������ݱ仯��֪��NOŨ�ȼ�С������Ũ�����ӣ�CO2Ũ�ȼ�С��˵��ƽ��������Ӧ�����ƶ������Ըı������Ǽ�СCO2��Ũ�ȡ�
��ԭ�����е�NO��N2��CO2��Ũ��֮��Ϊ4:3:3����˵�������¶�ƽ�����淴Ӧ�����ƶ����������Ӧ�Ƿ��ȷ�Ӧ��
��2�������˹���ɵ�Ӧ�ã����٣��ڣ��ۡ�4����2���õ�
CH4(g)+2NO2(g)==N2(g)+CO2(g)+2H2O(l)�����Է�Ӧ����
���D574kJ.mol-1�D1160kJ.mol-1�D-44.0kJ.mol-1��4����2����955kJ.mol-1��
��3����3���������ܸı�ƽ��״̬��A����ȷ��ѡ��B�з�Ӧ���ʵķ�Ӧ��ͬ��ʼ�ճ�����B����ȷ������Ӧ�Ƿ��ȷ�Ӧ�����������¶�ƽ�����淴Ӧ�����ƶ���ƽ�ⳣ����С��C��ȷ���÷�Ӧ���������Ŀ��淴Ӧ��ѡ��D�൱������ѹǿ������ƽ�����淴Ӧ�����ƶ���ת���ʽ��ͣ�D��ȷ����ѡCD��
��4������װ��ͼ��֪ʯī��ͨ��������������������ʯīI�Ǹ�����ʧȥ���ӣ���ӦʽΪNO2+NO3����e����N2O5��
�����Ѷȣ�һ��
4������� ��8�֣� A(g)+2B(g)  2C(g)�ķ�Ӧ�У�ʱ��t��C�����������C%���ĺ�����
2C(g)�ķ�Ӧ�У�ʱ��t��C�����������C%���ĺ�����
ϵ��ͼ��ʾ���ش��������⣺
��1��ͼA�����������߷ֱ��ʾ��100���400��ʱ��C%��ʱ��t�ĺ�����ϵ����P��ʾ���¶�Ϊ?�棬
��P��Q������ӦA(g)+2B(g)  2C(g)��?��Ӧ������ȡ����ȡ�����
2C(g)��?��Ӧ������ȡ����ȡ�����
��2��ͼB��P��ʾ���¶�Ϊ?�棬��ӦA(g)+2B(g)  2C(g)��?��Ӧ������ȡ����ȡ�����
2C(g)��?��Ӧ������ȡ����ȡ�����
�ο��𰸣���1��400��?���ȣ�2��100��?����
�����������1���¶ȸߣ���Ӧ���ʿ죬�ﵽƽ���ʱ���٣�P�������ȴﵽƽ��״̬������P��ʾ400�档�¶ȸߣ�C�ĺ���Ҳ�ߣ�˵�������¶ȣ�ƽ��������Ӧ�����ƶ�����������Ӧ�����ȷ�Ӧ��
��2������ͼ���֪��Q�������ȴﵽƽ��״̬������Q��ʾ����400�棬���P��ʾ����100�档�¶ȵͣ�C�ĺ����ߣ�˵�������¶ȣ�ƽ��������Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
�����Ѷȣ�һ��
5������� ��1����һ�������£��ݻ�Ϊ100L�ܱ������з�����Ӧ��CH4��g��+H2O��g��?CO��g��+3H2��g������H��0
��1.0molCH4��2.0molH2O��g��ͨ����ܱ�����l0minʱ��0.1molCO���ɣ���10min�ڸ÷�Ӧ��ƽ������v��H2��______��
��2����ѹǿΪ0.1MPa�����£��ݻ�ΪVLij�ܱ�������amolCO��2amolH2�ڴ��������·�Ӧ���ɼ״���CO��g��+2H2��g��?CH3OH��g����CO��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
�ٸ÷�Ӧ�ġ�H______�����������������=������
��100��ʱ�÷�Ӧ��ƽ�ⳣ��K=______���ú�a��V�Ĵ���ʽ��ʾ����
�����¶��ݻ����������£�����ܱ�����������amolCO��2amolH2���ﵽ��ƽ��ʱ��CO��ת����______�����������С�����䡱����ƽ�ⳣ��______�����������С�����䡱����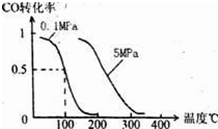
�ο��𰸣���1��l0minʱ��0.1molCO���ɣ�����v��CO��=0.1mol100L10min=0.0001mo1?L-1?min-1������֮�ȵ��ڻ�ѧ������֮�ȣ�����v��H2��=3v��CO��=3��0.0001mo1?L-1?min-1=0.0003mo1?L-1?min-1��
�ʴ�Ϊ��0.0003mo1?L-1?min-1��
��2������ͼ��֪��ѹǿ���䣬�¶�Խ��CO��ת����Խ�ͣ����¶�����ƽ�����淴Ӧ�����ƶ��������¶�ƽ�������ȷ�Ӧ�����ƶ�����������ӦΪ���ȷ�Ӧ������H��0��
�ʴ�Ϊ������
��100�棬ƽ��ʱCO��ת����Ϊ0.5�����Բμӷ�Ӧ��CO�����ʵ���Ϊ0.5amol��
���ڷ�Ӧ CO��g��+2H2��g��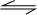 CH3OH��g����
CH3OH��g����
��ʼ��mol����a 2a 0
�仯��mol����0.5a a0.5a
ƽ�⣨mol����0.5a a 0.5a
����ƽ��ʱ CO��Ũ��Ϊ0.5amolvL=a2vmol/L��H2��Ũ��ΪamolvL=avmol/L��CH3OH��Ũ��Ϊ0.5amolvL=a2vmol/L��
100��ʱ�÷�Ӧ��ƽ�ⳣ��k=c(CH3OH)c(CO)?c2(H2)=a2va2v��(av)2=v2a2��
�ʴ�Ϊ��v2a2��
���¶��ݻ����䣬����ܱ�����������amolCO��2amolH2����ЧΪ��ʼ����2amolCO��4amolH2���������1����ƽ�������ѹǿ����ѹ���ָ���ԭ�����������ѹǿƽ���������С�ķ����ƶ����÷�ӦΪ���������С�ķ�Ӧ����������Ӧ�ƶ���COת��������
ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣮
�ʴ�Ϊ�������䣮
���������
�����Ѷȣ���