时间:2017-08-26 03:20:38
1、实验题 已知木炭在一定条件下与浓硝酸反应生成两种+4价的氧化物,为了探究一氧化氮(NO)能否与过氧化钠反应,以及反应后的产物中是否有亚硝酸钠(NaNO2),某小组同学设计了如图所示装置(夹持仪器和连接用的胶管已经省略)。
(1)①为了完成该实验,虚线框内还需要连接B~E四套装置,按气流方向连接的顺序为a?→(?)(?)→?(?)(?)→?(?)?(?)→?(?)(?)(填仪器接口的字母编号)。
②连接好仪器,检查气密性,装入药品后,要通入一段时间的氮气,再滴加浓硝酸,点燃酒精灯,通入氮气的主要目的是________________________。
(2)装置E中观察到的主要实验现象有_______________。
(3)装置C的作用是__________________。
(4)某同学经查阅资料后发现亚硝酸是弱酸,性质不稳定,室温下易分解成一氧化氮。装置D中充分反应后,设计实验证明D中是否有亚硝酸钠生成:_______________(写出检验步骤及现象)。
(5)亚硝酸钠在酸性条件下可将I-氧化为I2,该反应常用于亚硝酸钠含量的测定,请写出该反应的离子方程式:___________________。
参考答案:(1)hi→de→bc→fg(或gf);排除装置中的空气,防止一氧化氮被空气中的氧气氧化为二氧化氮
(2)溶液由无色变成蓝色,有无色气体逸出
(3)除去一氧化氮中的二氧化碳
(4)取少量D中的固体于试管中,加入稀硫酸,若溶液中有气泡产生且在试管液面上方变成红棕色气体,则D中有亚硝酸钠生成(或其他合理答案)
(5)2NO2+2I-+4H+=2NO+I2+2H2O
本题解析:
本题难度:一般
2、实验题 某些废旧塑料可采用下列方法处理:将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图所示。 
加热聚丙烯废旧塑料得到的产物如下表
(1)试管A中残余物质有多种用途,下列所示的转化就可制取高聚物聚乙炔。 
写出反应②③的化学方程式:_________________、__________________。?
(2)试管B中收集到的物质有两种,其中的一种能使酸性高锰酸钾溶液褪色,这种物质的一氯代物有_______种。 ?
(3)锥形瓶C中观察到的现象是________________________。?
(4)写出C中逸出的气体在工业上的两种用途:______________。
参考答案:(1)CaC2+2H2O→CH≡CH↑+Ca(OH)2、 nCH≡CH ?
?
(2)4?
(3)液体由橙色变为无色?
(4)用作燃料、用作化工原料
本题解析:
本题难度:一般
3、选择题 下列化学实验事实及其解释都正确的是:
A.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
B.向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO4难溶于盐酸
C.向0.1mol·L-1 FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有
氧化性
D.向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1 AgNO3溶液,
振荡,沉淀呈黄色,说明AgCl 的Ksp比AgI 的Ksp大
参考答案:AD
本题解析:B中的实验事实不存在,所以B不正确;
C 中的实验事实存在,解释错误,说明Fe2+具有还原性,所以C错误;
正确答案为AD。
本题难度:一般
4、填空题 Fe、Cu都是人类最早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
⑴ 甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到盛Cl2的集气瓶中。你认为甲同学在实验中应该观察到的现象是?;
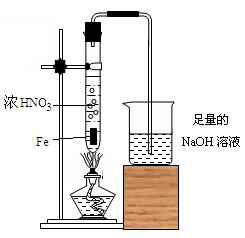
⑵ 乙同学为验证Fe能和热的浓HNO3反应,设计了如下图所示的实验装置,请你指出装置中的不足之处?;?;
?。
⑶ 丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解。
丙同学依据反应现象得出Cu片溶解的原因可能是和HNO3发生反应。他依据的反应现象是?;请写出Cu片和稀HNO3反应的离子方程式?
你认为Cu片溶解的不同于丙同学的理由是?
⑷ 请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象?
?。
参考答案:(1)Cu在Cl2中燃烧,产生棕色烟(1分)
(2)试管中的液体超过试管容积的三分之一(1分);加热液体的试管应与桌面成45°角向上倾斜而不应垂直向上(1分);尾气吸收装置容易发生倒吸(1分)
(3)①试管上部出现红棕色气体或无色气体(1分)?②3Cu+2NO3-+8 H+=3Cu 2++2NO+4 H2O (2分),反应产生的Fe3+也能和Cu反应而使Cu片溶解(2分)
(4)取该溶液少许,滴加适量的KSCN溶液,不出现血红色,再滴加适量新制氯水,出现血红色(2分)
本题解析:略
本题难度:简单
5、简答题 亚氯酸钠(NaClO2)主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解.以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
(1)提高“反应1”反应速率的措施有______、______等.
(2)“反应2”的氧化剂是______,该反应的化学方程式为:______.
(3)采取“减压蒸发”而不用“常压蒸发”,原因是______.
(4)从“母液”中可回收的主要物质是______.
(5)“冷却结晶”后经______(填操作名称)即可获得粗产品.
参考答案:(1)对伊气体和液体的反应,为提高反应速率,可适当升高反应温度;增大吸收液浓度,增大SO2与吸收液的接触面积,
故答案为:适当升高反应温度;增大吸收液浓度等;
(2)具有氧化性,根据生成NaClO2目标物的特点可知,反应的方程式为H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2,反应中Cl元素的化合价降低,则ClO2为氧化剂,
故答案为:ClO2;H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2;
(3)减压蒸发在较低温度下可进行,防止常压蒸发温度过高,亚硫酸钠容易分解,
故答案为:常压蒸发温度过高,亚硫酸钠容易分解;
(4)氯酸钠与二氧化硫在酸性条件下发生氧化还原反应生成ClO2和Na2SO4,则母液中应含有Na2SO4,
故答案为:Na2SO4;
(5)冷却结晶后要分离出固体,应用过滤的方法,故答案为:过滤.
本题解析:
本题难度:一般