ʱ��:2017-08-26 03:11:28
1��ѡ���� ��һ���¶��£���a L����̶����ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X(g) + 2Y(g)  3Z(g)������˵������ȷ����
3Z(g)������˵������ȷ����
A��������ѹǿ����ʱ��仯���仯
B��ijһʱ�̣������ڸ����ʵ�Ũ���п������
C���ﵽƽ��ʱ����λʱ��������3n mol Z��ͬʱ���� 2n mol Y
D��X��Y��ת�������
�ο��𰸣�B
���������A��ȷ���÷�ӦΪ�������Ӧ����Ӧǰ������������ʵ������䣬������ѹǿ���䡣
B����������X��Y�����ʵ���Ϊ1 mol X�����2 mol Y���壬�뻯ѧ��������ֵ��ȣ����ԣ�X��Y�����ʵ�ת������ȣ��仯������ȣ������ܻ����ijһʱ�̣������ڸ����ʵ�Ũ����ȵ������
C��ȷ����λʱ��������3n mol Z������Y2n mol����ͬʱ��������2n mol Y��Y��Ũ�Ȳ��䣬���ﵽ��ƽ�⣻
D��ȷ��X��Y��ת�������
�����Ѷȣ�һ��
2������� ��16�֣�I����CH4����ԭ��������������������������Ⱦ����֪��
��CH4��g��+4NO2��g��=4NO��g��+ CO2��g��+2H2O��g��? ��H=" -574" kJ��mol-l?
��CH4��g��+4NO��g��=2N2��g��+ CO2��g��+ 2H2O��g��? ��H=" -1160" kJ��mol-l
��H2O��g��=H2O��1��? ��H=-44��0 kJ��mol-l
д��CH4��g����NO2��g����Ӧ����N2��g����CO2��g����H2O��1�����Ȼ�ѧ����ʽ____?��
II����������Դ�����ϴ������ǿɳ�����չ����Ҫ���档
��1����̼��������Ӯ�Ӻϳ��Ҵ�ȼ���ѽ�����ģ���������ȡ��CO��H2Ϊԭ�Ϻϳ��Ҵ�����ѧ��Ӧ����ʽ��2CO��g��+4H2��g����CH3CH2OH��g��+H2O��g��;���ܱ������г���10 mol CO��20mol H2���ڴ��������·�Ӧ�����Ҵ���CO��ת���ʣ�a�����¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��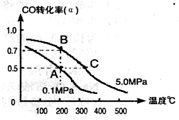
����A��B�����ʾ��ijʱ�̴ﵽ��ƽ��״̬����ʱ��A��ʱ���������Ϊ10L������¶��µ�ƽ�ⳣ����K=____?��
����A��C���㶼��ʾ�ﵽ��ƽ��״̬�����Ӧ��ʼ����ƽ��״̬�����ʱ��tA?tC���� ��>������<����=������
��2����ǰ��ҵ��Ҳ������CO2�������״���һ�������·�����Ӧ��CO2��g��+3H2��g��? ?CH3OH��g��+H2O��g����H<0������6mo1 CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���
?CH3OH��g��+H2O��g����H<0������6mo1 CO2��8mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���
�����ı�ijһʵ�������ٽ�������ʵ�飬���H2�����ʵ�����ʱ��仯��ͼ��������ʾ������I��Ӧ��ʵ�������ı������?������II��Ӧ��ʵ�������ı������____?��
�����ڴ����ͼ�л���״������ʵ�����ʱ��仯���ߡ�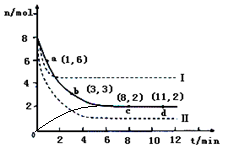
III����MnO2��KMnO4�Ĺ���������ͼ���������������Ͼ�Ϊ̼������ˮ��������Һ��K2MnO4�����绯�����MnO2��KMnO4��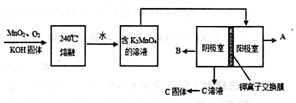
��д��240������ʱ������Ӧ�Ļ�ѧ����ʽ?��Ͷ��ʱ��������n��KOH��:n��MnO2��?��
�������ĵ缫��ӦΪ?��
��B������?���ѧʽ��������ѭ��ʹ�õ�������?���ѧʽ����
�ο��𰸣�28.��16�֣��� CH4(g)+2NO2(g) = N2(g) + CO2(g) +2H2O(l)? �SH=" -955" kJ��mol��1��2�֣�
��1����K="0.25" ��2�֣�? �� > ��1�֣�
��2�������£�1�֣���ѹ��1�֣������������𰸲��ո��֣�
������ͼ��2�֣�
�� 2MnO2 + O2 + 4KOH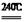 2K2MnO4 + 2H2O��2�֣�
2K2MnO4 + 2H2O��2�֣�
����2 : 1 ?(1��)
�� MnO42-?- e-?=? MnO4-?(2��)?
�� H2��1�֣�? KOH���� ��1�֣�
�����������(1)������ʽ����+��+�ۡ�4��/2��CH4��g����NO2��g����Ӧ����N2��g����CO2��g����H2O�ķ���ʽ���ʡ�H=��-574 -1160-44��0��4��/2= -955 kJ��mol��1����1����A��ʱCO��ת����Ϊ50����ת����Ϊ5mol����ƽ��ʱCO��H2��CH3CH2OH��H2O�����ʵ����ֱ�Ϊ5mol��10mol��2.5mol��2.5mol��ƽ��Ũ�ȷֱ�Ϊ0.5mol/L��1mol/L��0.25mol/L��0.25mol/L������ƽ�ⳣ������ʽK=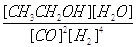 =0.25����C����¶ȸߣ���Ӧ���ʿ죬�ﵽƽ�����õ�ʱ��̣���2�������ߢ��ʵ����Ƚϣ��ӿ��˷�Ӧ���ʣ�ƽ�������ƶ��ˣ���Ϊ�����¶ȣ����ߢ��ʵ����Ƚϣ���Ӧ���ʼӿ죬ƽ�������ƶ��ˣ���Ϊ��ѹ���ڼ״������ʵ������㿪ʼ�����ﵽƽ��״̬ʱ��������6mol�����ɼ״�2mol���Ժ�״������ʵ������ٷ����仯�ˣ��������Ŀ��Ϣ�ɵ�ͨ���������̺�KOH����������������������K2MnO4�����ԭ���غ��������ԭ����ʽ����ƽ����д����ѧ����ʽ����KOH�Ͷ�������֮��Ϊ2:1ʱǡ����ȫ��Ӧ������ˮ��������Һ��K2MnO4�����绯�����MnO2��KMnO4���豣�ּ��Ի��������������ʵ���֮�ȴ���2:1��������MnO42-ʧȥ���ӷ���������Ӧ����MnO4- ����ΪMnO42-?- e-?=? MnO4- �������������ӵõ�������������ͬʱ�����������أ��������ؿ���ѭ��ʹ�á�
=0.25����C����¶ȸߣ���Ӧ���ʿ죬�ﵽƽ�����õ�ʱ��̣���2�������ߢ��ʵ����Ƚϣ��ӿ��˷�Ӧ���ʣ�ƽ�������ƶ��ˣ���Ϊ�����¶ȣ����ߢ��ʵ����Ƚϣ���Ӧ���ʼӿ죬ƽ�������ƶ��ˣ���Ϊ��ѹ���ڼ״������ʵ������㿪ʼ�����ﵽƽ��״̬ʱ��������6mol�����ɼ״�2mol���Ժ�״������ʵ������ٷ����仯�ˣ��������Ŀ��Ϣ�ɵ�ͨ���������̺�KOH����������������������K2MnO4�����ԭ���غ��������ԭ����ʽ����ƽ����д����ѧ����ʽ����KOH�Ͷ�������֮��Ϊ2:1ʱǡ����ȫ��Ӧ������ˮ��������Һ��K2MnO4�����绯�����MnO2��KMnO4���豣�ּ��Ի��������������ʵ���֮�ȴ���2:1��������MnO42-ʧȥ���ӷ���������Ӧ����MnO4- ����ΪMnO42-?- e-?=? MnO4- �������������ӵõ�������������ͬʱ�����������أ��������ؿ���ѭ��ʹ�á�
�����Ѷȣ�һ��
3��ѡ���� ��Ӧ4NH3��������5O2������ 4NO��������6H2O��������10L�ܱ������н��У�����Ӻ�ˮ���������ʵ���������0.45mol����˷�Ӧ��ƽ������
4NO��������6H2O��������10L�ܱ������н��У�����Ӻ�ˮ���������ʵ���������0.45mol����˷�Ӧ��ƽ������ (X)(��Ӧ����������ʻ�������������)�ɱ�ʾΪ
(X)(��Ӧ����������ʻ�������������)�ɱ�ʾΪ
[? ]
A�� (NH3)=0.0101mol��L-1��s-1
(NH3)=0.0101mol��L-1��s-1
B�� (O2)=0.0010 mol��L-1��s-1
(O2)=0.0010 mol��L-1��s-1
C��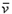 (NO)=0.0010 mol��L-1��s-1
(NO)=0.0010 mol��L-1��s-1
D�� (H2O)=0.045 mol��L-1��s-1
(H2O)=0.045 mol��L-1��s-1
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ���淴Ӧ ���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ�?��
���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ�?��
A��NO2ȫ�������NO��O2
B����Ӧ�Ѿ�ֹͣ��
C����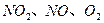 �����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
D����λʱ��������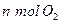 ��ͬʱ����
��ͬʱ����
�ο��𰸣�D
�����������
�����Ѷȣ���
5������� ��7�֣�����ͼ��ʾ�������ݻ���ͬ�����������١��ڡ����н������µķ�Ӧ��
3A(g) + B(g) 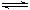 ?2C(g)����H��0
?2C(g)����H��0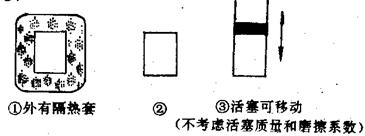
��1������ʼ�¶���ͬ���ֱ������������г���3 mol A��1 mol B����ﵽƽ��ʱ��������C���ʵİٷֺ����ɴ�С��˳��Ϊ����������ţ�?��
��2����ά���¶Ȳ��䣬��ʼʱ�� �����о�Ͷ��3 mol A��1 mol B����ﵽƽ��ʱ����������C���ʵ����ʵ���Ũ�Ȣ�?�ۣ���<��>��=����
�����о�Ͷ��3 mol A��1 mol B����ﵽƽ��ʱ����������C���ʵ����ʵ���Ũ�Ȣ�?�ۣ���<��>��=����
��3���ڢ���Ͷ��3 mol A��1 mol B��ƽ�⣻������ͬ�����£���ʼʱ�ڢ���Ͷ��a mol A��b mol B��c mol C��ʹ���������ƽ��ʱ������C�İٷֺ�����ȣ���a��b��c�Ĺ�ϵΪ?��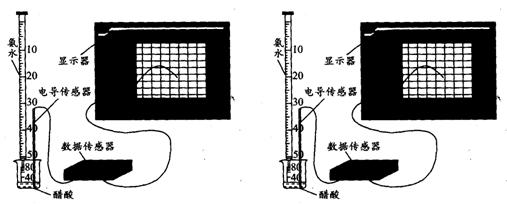
�ο��𰸣�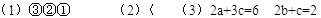
�����������
�����Ѷȣ�һ��