时间:2017-08-26 03:09:37
1、简答题 将黑色固体单质甲在酒精灯火焰上灼烧至红热后,投入无色溶液乙中,甲跟乙经剧烈反应后生成含有红棕色的气态混合物A,将A隔绝空气,按如图发生一系列变化.完成下面问题.(提示:已知b溶液是乙的稀溶液,气体A、a均为混合气体) 
(1)甲为______,乙为______,丙为______.
(2)混合气体A的主要成分有______.
(3)气体B是______,蓝色溶液C是______.
(4)甲跟乙反应的化学方程式是______.
参考答案:溶液b为是乙的稀溶液,与单质丙反应可以得到蓝色溶液C,则C溶液含有铜离子,结合转化关系可知,丙为Cu、乙为硝酸,故C为Cu(NO3)2,反应生成气体B为NO.黑色固体单质甲跟乙经剧烈反应后生成含有红棕色的气态混合物A,可推知A为CO2、NO2混合气体,甲为碳单质.A隔绝空气,通入水中得到混合气体a为CO2、NO,与足量的石灰水反应得到白色沉淀与NO,则白色沉淀为CaCO3,
(1)由上述分析可知,甲为:碳,乙为Cu(NO3)2,丙为Cu,故答案为:碳;Cu(NO3)2;Cu;
(2)由上述分析可知,A为CO2、NO2混合气体,故答案为:CO2、NO2;
(3)由上述分析可知,B为NO,蓝色溶液C是Cu(NO3)2,故答案为:NO;Cu(NO3)2;
(4)单质碳与浓硝酸反应的化学方程式为:C+4HNO3(浓)△.CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)△.CO2↑+4NO2↑+2H2O.
本题解析:
本题难度:简单
2、填空题 如图中各物质均由短周期元素组成,其中只有D、F、G为单质,A为淡黄色固体,B为常见的无色液体,一定条件下D、G和海水为原料可制成海洋电池.按要求填空:
(1)写出电子式A______;?B______;
(2)写出化学方程式①______;②______;
(3)写出D、G和海水制成海洋电池的负极反应式______.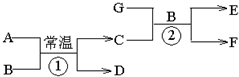
参考答案:各物质均由短周期元素组成,A为淡黄色固体,B为常见的无色液体,则A为Na2O2,B为H2O,D、F、G为单质,由转化关系图可知,D为氧气,G为Al,F为氢气,
(1)A为Na2O2,其电子式为
,B为H2O,其电子式为
,
故答案为:
;
;
(2)转化中①为过氧化钠与水的反应,该反应为2Na2O2+2H2O=4NaOH+O2↑,反应②为Al与NaOH溶液的反应,该反应为2Al+2NaOH+2H2O=2Al+2NaOH+3H2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;2Al+2NaOH+2H2O=2Al+2NaOH+3H2↑;
(3)D为氧气,G为Al,与海水构成的原电池中Al作负极,负极反应式为Al-3e-=Al3+,故答案为:Al-3e-=Al3+.
本题解析:
本题难度:简单
3、填空题 A、B、C、D、E、F、X存在如图所示转换关系,其中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。X可能是强酸,也可能是强碱。
(1)A的化学式是___________________。
(2)若X是强酸,将D与Cl2同时通入水中发生反应的离子方程式为_____________________________。
(3)若X是强碱,过量的B跟Cl2反应除生成C外,另一产物是氯化物。
①过量的B跟Cl2反应的化学方程式为______________________。
②工业生产中B→D的化学方程式为_______________________。
参考答案:(1)(NH4)2S(2分) (2)Cl2+SO2+2H2O=4H++SO42-+2Cl-(2分)
(3)①3Cl2+8NH3=N2+6NH4Cl(2分) ②4NH3+5O2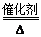 4NO+6H2O(2分)
4NO+6H2O(2分)
本题解析:
试题分析:(1)正盐A既能和强酸反应生成氢化物,也能喝强碱反应生成氢化物,则A一定是弱酸的铵盐。E能和水反应生成强酸F,因此E是NO2或三氧化硫。则A是硫化铵,化学式为(NH4)2S。
(2)若X是强酸,则B是H2S。H2S被氯气氧化生成单质硫,即C是S。所以D是SO2,E是三氧化硫,F是硫酸。氯气具有氧化性,能把SO2氧化生成硫酸,所以将D与Cl2同时通入水中发生反应的离子方程式为Cl2+SO2+2H2O=4H++SO42-+2Cl-。
(3)若X是强碱,则B是氨气。氨气被氯气氧化生成氮气,所以C是氮气。则D是NO,E是NO2。
①氯气氧化氨气生成氮气和氯化氢,过量的氨气跟氯化氢反应生成氯化铵,因此过量的B跟Cl2反应的化学方程式为3Cl2+8NH3=N2+6NH4Cl。
②工业生产中B→D所以氨的催化氧化,反应的化学方程式为4NH3+5O2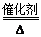 4NO+6H2O。
4NO+6H2O。
本题难度:一般
4、推断题 氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空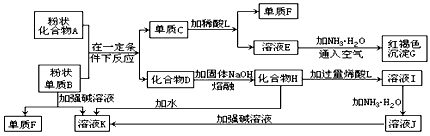
(1)单质F是________。
(2)写出由E生成G的离子反应方程式_____________________。
(3)溶液I中所含金属离子是______。
(4)由C→E+F若改用浓酸,则不能选用的浓酸________。
参考答案:(1)H2
(2)4Fe2++8NH3・H2O+O2+2H2O==4Fe(OH)3↓+8NH4+(或分两步写出:①Fe2++2NH3・H2O==Fe(OH)2↓+
2NH4+ ②4Fe(OH)2+O2+2H2O==4Fe(OH)3↓)
(3)Al3+和Na+
(4)H2SO4(或HNO3)
本题解析:
本题难度:一般
5、选择题 已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如图转化关系,Z是NO,下列推断不合理的是( )
A.X可能是一种氢化物
B.若Y为单质,Y生成Z属于化合反应
C.E可能是一种有色气体
D.F中M元素的化合价可能为+5
参考答案:B
本题解析:
本题难度:一般