时间:2017-08-26 03:01:28
1、填空题 有下列四种溶液(均无气体逸出) ?
A.0.01mol/L的H2CO3溶液 ?
B.0.01mol/L的NaHCO3溶液 ?
C.0.02mol/L的HCl与0.04mol/L的NaHCO3溶液等体积混合液 ?
D.0.02mol/L的NaOH与0.02?mol/L的NaHCO3溶液等体积混合液
据此,填写下列空白(填代号)?
(1)?c(H+)?最大的是______________;?
(2)?c(H2CO3)?最大的是______________; ?
(3)?c(HCO3-)?最大的是____________;
(4)?c(CO32-)?最大的是_____________?;
(5)?c(HCO3-)?最小的是____________。
参考答案:(1)A?
(2)D
(3)D
(4)C?
(5)A
本题解析:
本题难度:一般
2、选择题 常温下的下列混合溶液中,各离子浓度的大小顺序正确的是( )
A.10mLpH=13的氨水与10mLpH=1的盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.10mL0.1mol/LNH4Cl溶液与5mL0.2mol/LNaOH溶液混合:c(Cl-)=c(Na+)>c(OH-)>c(H+)
C.10mL0.1mol/LCH3COOH溶液与10mLpH=13的NaOH混合:c(CH3COO-)=c(Na+)>c(OH-)>c(H+)
D.10mL0.5mol/LCH3COONa溶液与6mLpH=0的盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+)
参考答案:A、pH=13的氨水其浓度大于0.1mol/L,pH=1的盐酸其浓度为0.1mol/L,则混合后溶液中的溶质为氯化铵和一水合氨,一水合氨的电离大于铵根离子的水解,则c(NH4+)>c(Cl-),故A错误;
B、10mL0.1mol/LNH4Cl溶液与5mL0.2mol/LNaOH溶液中溶质的物质的量相等,钠离子和氯离子的物质的量浓度相等,该溶液为碱与盐的混合溶液,则显碱性,即c(OH-)>c(H+),又部分氢氧根离子结合铵根离子,则c(Na+)>c(OH-),故B正确;
C、10mL0.1mol/LCH3COOH溶液与10mLpH=13的NaOH溶液中溶质的物质的量相等,恰好完全反应后溶液中的溶质只有醋酸钠,由醋酸根离子水解可知c(Na+)>c(CH3COO-),故C错误;
D、10mL0.5mol/LCH3COONa溶液与6mLpH=0的盐酸中溶质的物质的量的关系为5:6,则c(Cl-)>c(Na+),但盐与酸的混合溶液显酸性,则c(H+)>c(OH-),故D错误;
故选B.
本题解析:
本题难度:简单
3、选择题 下列物质中,不属于电解质的是
A.苏打
B.食盐
C.硫酸
D.蔗糖
参考答案:D
本题解析:溶于水或在熔融状态下能导电的化合物是电解质,在上述条件下都不能导电的化合物是非电解质,所以A、B、C都是电解质,蔗糖是非电解质,答案选D。
点评:判断电解质或非电解质时,需要注意的是导电只是一种现象,关键是看化合物能不能自身电离出离子,溶于水或在熔融状态下能自身电离出离子的化合物是电解质,不能电离出离子的化合物是非电解质。
本题难度:简单
4、选择题 现有常温下的四种溶液(如下表),下列有关叙述中正确的是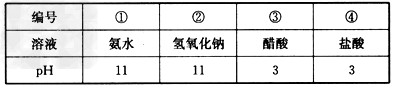
[? ]
A.在①、②中分别加入适量的氯化铵固体后,①的pH减小,②的pH不变
B.温度下降10℃,四种溶液的pH均不变
C.分别加水稀释10倍,四种溶液的pH:①>②>④>③
D.将①、④两种溶液等体积混合,所得溶液中:c(NH4+)> c(Cl-)>c(H+)>c(OH-)
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列物质的水溶液能导电,但属于非电解质的是
[? ]
参考答案:D
本题解析:
本题难度:简单