时间:2017-08-26 02:17:31
1、选择题 室温时,某醋酸溶液的pH=3,其中的c(OH-)是( )
A.1×10-3mol/L
B.1×10-7mol/L
C.1×10-11mol/L
D.无法确定
参考答案:室温时,某醋酸溶液的pH=3,pH=-lgc(H+),所以c(H+)=1×10-3mol/L,室温时,Kw=c(OH-)×c(H+)=1×10-14,根据Kw=c(OH-)×c(H+),c(OH-)=10-1410-3mol/L=1×10-11mol/L,
故选:C.
本题解析:
本题难度:一般
2、选择题 pH=3的盐酸用水稀释,体积变为原体积的2倍后,这时溶液的pH接近于(已知lg2=0.3、lg3=0.5、lg5=0.7)
[? ]
A.1.5
B.3.3
C.3.5
D.2.7
参考答案:B
本题解析:
本题难度:一般
3、选择题 把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混合,则混合液中微粒浓度关系正确的是( )
A.c?(CH3COO-)>c?(Na+)
B.c?(CH3COOH)+c?(CH3COO-)=0.02mol/L
C.c?(CH3COOH)>c?(CH3COO-)
D.c?(OH-)>c?(H+)
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列叙述正确的是
[? ]
A.某氨水溶液的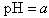 ,将此溶液稀释10倍后,溶液的
,将此溶液稀释10倍后,溶液的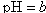 ,则b + 1= a
,则b + 1= a
B.在滴有酚酞溶液的氨水里,加入![]() 至溶液恰好无色,则此时溶液的pH = 7
至溶液恰好无色,则此时溶液的pH = 7
C.![]() 醋酸的
醋酸的![]() ,
,![]() 盐酸的pH小于7且接近7
盐酸的pH小于7且接近7
D.若1mL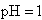 的盐酸与100mL
的盐酸与100mL![]() 溶液混合后,溶液
溶液混合后,溶液![]() 的则
的则![]() 溶液的
溶液的![]()
参考答案:D
本题解析:
本题难度:一般
5、选择题 现有常温下pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是( )
A.加入10mL0.01mol/L的NaOH溶液
B.加入10mL的水进行稀释
C.加水稀释成100mL
D.加入10mL0.01mol/L的盐酸
参考答案:C
本题解析:
本题难度:一般