时间:2017-08-26 01:44:25
1、选择题 常温下,在0.01 mol・L―1的H2SO4溶液中,由水电离出来的c(H+)是:
A.5×10-13 mol・L―1;
B.0.02 mol・L―1;
C.1.00×10-7 mol・L―1;
D.1.00×10-12 mol・L―1
2、填空题 I.(1)CH3OH(1)、H2的燃烧热分别为:725.5 kJ/mol和285.8 kJ/mol,写出工业上以CO2、H2合成CH3OH(1)的热化学方程式:?。
(2)右图为光电解水的装置,写出光照时半导体电极表面发生的电极反应式________。目前应用最多的半导体材料是Si,甚至有人提出硅是“21世纪的能源”,硅可作为新能源的原因可能的是?(填字母)。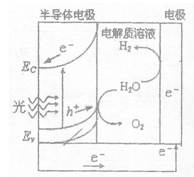
a.在自然界中存在大量的单质硅?
b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多
d.硅的化学性质不活泼,便于安全贮存、运输
II.将0.2mol/L HA溶液与O.lmol/L NaOH溶液等体积混合,测得混合溶液c(Na+)>c(A―),
用“>”、“<”或“=”填写下列空白:
(1)混合溶液中c(A―)____c(HA);c(HA)+c(A―)__0.lmol/L;
(2)混合溶液中,由水电离出来的c(OH―)?0.2mol/L HA溶液中由水电离出的c(H+)
(3)25℃时,如果取0.2mol/L HB溶液与0.lmol/L NaOH溶液等体积混合,测得混合溶液的pH <7,则HB的电离程度?NaB的水解程度。
3、选择题 下列操作会使H2O的电离平衡向电离方向移动且pH<7的是
A.向水中加少量Na2CO3
B.向水中加少量FeCl3
C.向水中加少量NaHSO4
D.向水中加入少量NaCl
4、选择题 现有物质的量浓度均为0.1 mol/L的下列5种物质的水溶液:①HNO3?②H2SO4③CH3COOH?④? NaOH其溶液中由水电离出的c(H+)的大小关系是
A.③>①=④>②
B.③=①=④>②
C.②>①>③>④
D.③>①>④>②
5、选择题 下列各组物质的燃烧热相等的是 ( )
A.红磷和白磷
B.1g H2和2g H2
C.3molC2H2和1molC6H6
D.葡萄糖和果糖