时间:2017-08-26 00:57:04
1、选择题 某反应的反应过程和能量变化如图所示,下列有关该反应的叙述正确的是( )
A.该反应的反应热△H<0
B.反应物的总能量低于生成物的总能量
C.该反应是吸热反应
D.加入催化剂后反应放出的热会减少
2、选择题 由图分析,下列说法正确的是

[? ]
3、选择题 以下反应可用焓判据来解释的是
[? ]
4、选择题 已知:H+(aq)+OH-(aq)==H2O(l);△H=-57.3 kJ・mol-1。现将一定量的稀盐酸、浓硫酸、稀醋酸分别和
1L 1mol・L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2和△H3的大小关系为
[? ]
A. △H1=△H2>△H3
B. △H3>△H2>△H1
C. △H3>△H1>△H2
D. △H2>△H1>△H3
5、填空题 (16分)工业上可用煤制天然气,生产过程中有多种途径生成CH4。
(1)写出CO2与H2反应生成CH4和H2O的热化学方程式??。
已知:?① CO(g)+H2O(g) H2(g)+CO2(g)? ΔH=-41kJ・mol-1?
H2(g)+CO2(g)? ΔH=-41kJ・mol-1?
② C(s)+2H2(g) CH4(g)?ΔH=-73kJ・mol-1
CH4(g)?ΔH=-73kJ・mol-1
③ 2CO(g) C(s)+CO2(g)?ΔH=-171kJ・mol-1
C(s)+CO2(g)?ΔH=-171kJ・mol-1
(2)另一生成CH4的途径是CO(g)+3H2(g) CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。
CH4(g)+H2O(g)。其他条件相同时,H2的平衡转化率在不同压强下随温度的变化如图所示。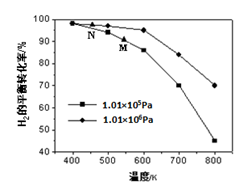
①该反应的△H?0(填“<”、“=”或“>”)。
②实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由________________________。
③某温度下,将0.1 mol CO和0.3 mol H2充入10L的密闭容器内发生反应CO(g)+3H2(g)  CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)
CH4(g)+H2O(g),平衡时H2的转化率为80%,求此温度下该反应的平衡常数K。(写出计算过程,计算结果保留两位有效数字)