时间:2017-08-26 00:56:41
1、选择题 在研究合成氨方法的历史上,不同的研究者曾3次获诺贝尔化学奖。合成氨大大提高了农作物的产量,同时也是制取硝酸、炸药等的原料。下列说法中正确的是
A.N2和H2在点燃或光照条件下可合成氨气
B.氨和HNO3都是电解质
C.氨气遇到浓硝酸会发生反应产生大量白烟
D.由NH3制HNO3的过程中,氮元素被还原
2、选择题 将下列气体通入水中,既能生成含氧酸,又能生成无氧酸的是:(?)
A.氯气
B.二氧化氮
C.硫化氢
D.二氧化碳
3、选择题 下列说法正确的是
A.臭氧与氧气互为同位素
B.蛋白质属于有机高分子化合物,其水溶液能通过半透膜
C.氨易液化的主要原因是氨分子间易形成氢键
D.水泥、玻璃、玛瑙均属于硅酸盐材料
4、选择题 已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是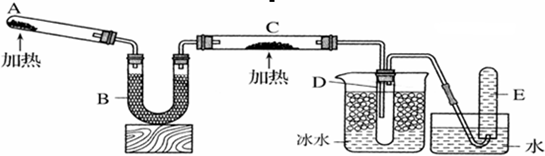
A.反应中氧化剂和还原剂的物质的量之比为2∶3
B.装置B中加入的物质可以是碱石灰或无水氯化钙
C.装置D中液体可以使干燥的红色石蕊试纸变蓝
D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气
5、填空题 (10分)三氟化氮是一种无色、无味、无毒且不可燃的气体,可在铜的催化作用下由F2和过量NH3反应得到,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO 和 HNO3,请根据要 求回答下列问题:
求回答下列问题:
⑴写出制备NF3的化学反应方程式:?。反应过程中,氧化剂与还原剂的物质的量之比为?。
⑵写出三氟化氮与水蒸气反应的化学方程式:?。⑶NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体
泄漏时的现象是?。
⑷一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种
钠盐:?(填化学式)。