时间:2017-08-26 00:38:13
1、选择题 已知常温下CH3COOH的电离平衡常数为Ka,常温下,向20mL 0.1 mol・L-1CH3COOH溶液中逐滴加入0.1 mol・L-1NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是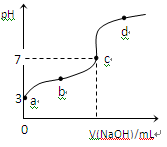
A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol・L-1
B.b点表示的溶液c(CH3COO-) > c(Na+)
C.c点表示CH3COOH和NaOH恰好反应完全
D.b、d点表示的溶液中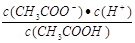 相等
相等
参考答案:C
本题解析:
答案C
恰好完全反应时,产物为CH3COONa,是强碱弱酸盐,水解后溶液呈碱性,pH>7
本题难度:一般
2、选择题 25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH的关系如图所示。下列有关溶液中离子浓度关系叙述正确的是?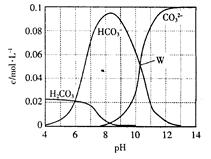
A.W点所示的溶液中:c (Na+)+c (H+)="2c" (CO32― )+c (OH― )+c (Cl― )
B.pH= 4的溶液中:c (H2CO3)+c (HCO3―)+c (CO32―)<0.1mol・L―1
C.pH=8的溶液中:c (H+)+c (H2CO3)+c (HCO3―)=" c" (OH― )+c (Cl― )
D.pH=11的溶液中:c (Na+)>c (Cl― )>c (CO32― )>c (HCO3― )>c (H2CO3)
参考答案:B
本题解析:根据电荷守恒可知,溶液中离子应该满足关系式c(Na+)+ c(H+)=2c(CO32-)+ c(OH-)+ c(Cl-) + c(HCO3-),A不正确;pH=4,说明反应中有CO2生成,所以根据物料守恒可知c(H2CO3)+ c(HCO3-)+ c(CO32?-)<0.1 mol・L-1,B正确;根据图像可知pH=8时,溶液中碳酸氢钠的远远大于碳酸钠的浓度,这说明反应中恰好是生成碳酸氢钠,则根据物料守恒可知c(H2CO3)+ c(HCO3-)+ c(CO32?-)=c(Cl-)=1/2 c(Na+),则c(H+)+ 2c(H2CO3)+ 2c(HCO3-) = c(OH-)+c(Cl-),C不正确;根据图像可知pH=11时,溶液碳酸钠的浓度远远大于碳酸氢钠的浓度,这说明碳酸钠是过量的,则c(Na+)>c(CO32?-) >c(Cl-)>c(HCO3-)>c(H2CO3),D不正确,答案选B。
点评:该题是高考中的常见题型,属于综合性试题的考查,对学生的思维能力提出了较高的要求,本题贴近高考,综合性强,侧重对学生能力的培养,意在培养学生的逻辑推理能力和创新思维能力。该题的关键是在明确反应原理的基础上利用好几种守恒关系,即电荷守恒、物料守恒以及质子守恒,然后结合图像和题意灵活运用即可。
本题难度:一般
3、选择题 对100mL 1mol・L-1的Na2CO3溶液,下列说法不正确的是
A.将溶液稀释,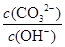 减少
减少
B.滴人含0.l mol CH3COOH的溶液:c ( CH3 COO一)<c( HCO3一)
C.通人0.1 mo1CO2气体,溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3)
D.滴人酚酞,微热,溶液颜色加深
参考答案:B
本题解析:A、碳酸钠溶液中CO32-水解,稀释促进水解,因此CO32-的物质的量减少和OH-的物质的量增加,所以将溶液稀释,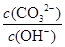 减少,A正确;B、滴人含0.l mol CH3COOH的溶液中二者反应恰好生成碳酸氢钠和醋酸钠,由于醋酸的酸性强于碳酸的,因此醋酸钠的水解程度小于碳酸氢钠的水解程度,所以溶液中c ( CH3 COO一)>c( HCO3一),B不正确;C、通人0.1 mo1CO2气体,二者恰好反应生成碳酸氢钠,根据物料守恒可知溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3),C正确;D、水解吸热,滴人酚酞,微热,促进水解,溶液碱性增强,因此溶液颜色加深,D正确,答案选B。
减少,A正确;B、滴人含0.l mol CH3COOH的溶液中二者反应恰好生成碳酸氢钠和醋酸钠,由于醋酸的酸性强于碳酸的,因此醋酸钠的水解程度小于碳酸氢钠的水解程度,所以溶液中c ( CH3 COO一)>c( HCO3一),B不正确;C、通人0.1 mo1CO2气体,二者恰好反应生成碳酸氢钠,根据物料守恒可知溶液中存在:c ( Na+)=c( CO32一)十c( HCO3一)+c(H2CO3),C正确;D、水解吸热,滴人酚酞,微热,促进水解,溶液碱性增强,因此溶液颜色加深,D正确,答案选B。
本题难度:一般
4、填空题 已知溶液中只存在OH-、H+、Na+、CH3COO-四种离子,试回答下列问题:
(1)若溶液中只溶解了一种溶质,则该溶质是?,溶液中c(H+)?c(OH-)(填“>”、“=”或“<”)。
(2)若溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),则该溶液中的溶质为?,若溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则该溶液中溶质为?。
(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,且恰好呈中性,则混合前c(NaOH)?c(CH3COOH),混合前碱中c(OH-)和酸中c(H+)的关系c(OH-)?c(H+)(填“>”,“=”或“<”)。
参考答案:(1)CH3COONa ;?< ;?(2)NaOH和CH3COONa;? CH3COOH和CH3COONa, (3)<?>
本题解析:(1)若溶液中只溶解了一种溶质,则该溶质是CH3COONa.由于CH3COON a是强碱弱酸盐。弱酸根离子水解CH3COO-+H2O CH3COOH+OH-,消耗了水电离产生的H+,破坏了水的电离平衡,水会继续电离产生的H+又被消耗,最终当达到电离平衡时,c(H+)<c(OH-)。(2)若溶液中只存在溶质CH3COONa,则由于CH3COO-水解消耗,所以 c(Na+)> c(CH3COO-);Na+、CH3COO-都是盐电离产生的,而OH-、H+都是弱电解质水电离产生的。盐的电离远大于水的电离。则c(CH3COO-)>c(OH-)。这与题意不符。说明溶液中还存在其它的电解质。由于c(OH-)>c(CH3COO-),说明还存在碱NaOH。因此该溶液中的溶质为NaOH和CH3COONa。若溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则说明溶液显酸性,含有溶质CH3COOH。由于溶液中c(CH3COO-)>c(Na+),则还有溶质CH3COONa。因此该溶液中的溶质为CH3COOH和CH3COONa。(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,若二者的物质的量相等,则溶液显碱性。性质溶液恰好呈中性,则说明混合前n(CH3COOH)>n(NaOH).由于NaOH是强碱,完全电离,而CH3COOH是弱酸,部分电离,混合前碱中c(OH-)和酸中c(H+)的关系c(OH-)>c(H+)。
CH3COOH+OH-,消耗了水电离产生的H+,破坏了水的电离平衡,水会继续电离产生的H+又被消耗,最终当达到电离平衡时,c(H+)<c(OH-)。(2)若溶液中只存在溶质CH3COONa,则由于CH3COO-水解消耗,所以 c(Na+)> c(CH3COO-);Na+、CH3COO-都是盐电离产生的,而OH-、H+都是弱电解质水电离产生的。盐的电离远大于水的电离。则c(CH3COO-)>c(OH-)。这与题意不符。说明溶液中还存在其它的电解质。由于c(OH-)>c(CH3COO-),说明还存在碱NaOH。因此该溶液中的溶质为NaOH和CH3COONa。若溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则说明溶液显酸性,含有溶质CH3COOH。由于溶液中c(CH3COO-)>c(Na+),则还有溶质CH3COONa。因此该溶液中的溶质为CH3COOH和CH3COONa。(3)若该溶液是由体积相等的NaOH溶液和醋酸溶液混合而成,若二者的物质的量相等,则溶液显碱性。性质溶液恰好呈中性,则说明混合前n(CH3COOH)>n(NaOH).由于NaOH是强碱,完全电离,而CH3COOH是弱酸,部分电离,混合前碱中c(OH-)和酸中c(H+)的关系c(OH-)>c(H+)。
本题难度:一般
5、选择题 下列说法正确的是
A.室温下,pH之和为14的氨水与盐酸等体积混合,溶液一定呈中性
B.在0.1 mol/L(NH4)2Fe(SO4)2溶液中
c(H+)+c(NH4+)+2c(Fe2+)=c(OH-)+c(SO42-)
C.向醋酸溶液中加入适量醋酸钠,所得酸性溶液中
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.0.4 mol/L HCl与0.1 mol/L NaAlO2等体积混合,所得溶液中:
?c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-)
参考答案:D
本题解析:
A.不正确,室温下,pH之和为14的氨水与盐酸等体积混合,溶液不一定呈中性,如氨水为弱碱,pH=4的盐酸和pH=l0的氨水中,氨水过量,反应后溶液呈碱性;
B.不正确,在0.1 mol/L(NH4)2Fe(SO4)2溶液中存在电荷守恒:
?c(H+)+c(NH4+)+2c(Fe2+)=c(OH-)+2c(SO42-)
C.不正确,向醋酸溶液中加入适量醋酸钠,所得酸性溶液中
?c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.正确,0.4 mol/L HCl与0.1 mol/L NaAlO2等体积混合,所得溶液为AlCl3:Al3+水解比Na+少,?c(Cl-)>c(Na+)>c(Al3+)>c(H+)>c(OH-)
选D。
本题难度:一般