时间:2017-08-22 17:05:46
1、简答题 如图中A~H均为中学化学中常见的物质,它们之间有如下转化关系.其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、H的焰色反应均呈黄色,在通常状况下E(氢氧化物)跟NaOH或盐酸均可发生复分解反应(反应过程中生成的水及其他产物已略去).
请回答以下问题:
(1)B是______,H是______.(填化学式)
(2)写出E转化为G的离子方程式______.
(3)A在常温下也可与D溶液反应生成G,写出此反应的化学方程式______.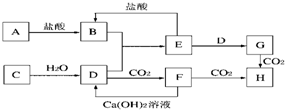
2、推断题 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出):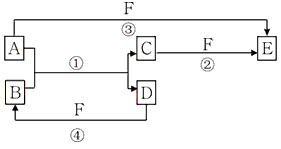
(1)若A、D、F都是短周期非金属元素单质,且A、D常温下为固态单质,所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为_________________________;B固体的晶体类型属于__________晶体。写出E的结构式_________。
(2)若A是常见的金属单质,常温下D、F是气态单质,反应①和②均在水溶液中进行。用离子方程式解释E的水溶液显酸性原因____________________________,D与F在一定条件下反应生成B的化学方程式为_____________________________。
(3)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,③与④两个反应中都有红棕色气体生成(部分产物框图中未给出),则A的原子结构示意图为
_________,D在周期表中位置______________,反应①的化学方程式为_________________________。
3、填空题 阅读下表中短周期主族元素的相关信息。
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都要有E元素 |
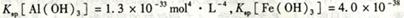 mol4・L一4。现向pH=0,浓度均为0.04mol・L-1的Al3+、Fe3+溶液中加入A的最高价氧化物对应水化物的溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是
mol4・L一4。现向pH=0,浓度均为0.04mol・L-1的Al3+、Fe3+溶液中加入A的最高价氧化物对应水化物的溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是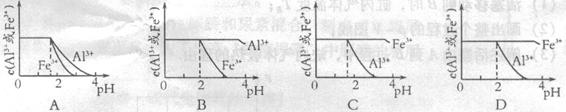
4、填空题 有关元素X、Y、Z、W的信息如下:
请回答下列问题:
(1) Y的单质在空气 中充分燃烧所得氧化物的电子式________________
中充分燃烧所得氧化物的电子式________________
(2) X、Y、W的简单离子的半径由大到小的是_______________ (写离子符号)
(3) 向淀粉碘化钾溶液中滴加几滴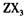 的浓溶液,现象为______________ ,
的浓溶液,现象为______________ ,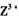 基态离子的电子排布式为?
基态离子的电子排布式为?
(4) 以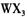 溶液为原料制取无水
溶液为原料制取无水 ,主要操作包括加热浓缩、冷却结晶、过滤,先制得
,主要操作包括加热浓缩、冷却结晶、过滤,先制得 晶体,然后在条件下加热
晶体,然后在条件下加热 晶体,能进一步制取无水
晶体,能进一步制取无水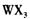 .其原因是(结合离子方程式简要说明)? _____________________________________________
.其原因是(结合离子方程式简要说明)? _____________________________________________
5、填空题 化合物X、Y、Z是由短周期的三种元素两两结合而成,X、Y、Z之间的转化关系如右图所示(无被省略的物质):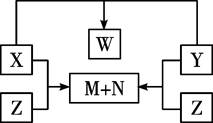
又知:X、N、W均为液态物质,且X与N的组成元素相同。试回答:
(1)上述转化关系图中涉及的基本反应类型是?;
(2)X、Y、Z、W的化学式依次是:
X?、Y?、Z?、W?;
(3)写出X与Y、X与Z反应的化学方程式:
X+Y:?;
X+Z:?。