时间:2017-08-22 17:00:57
1、选择题 某化学式为AB的离子晶体,已知5r(A2+)=4r(B2-)(各类离子晶体与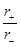 关系如下图所示),经测定其密度为
关系如下图所示),经测定其密度为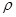 g・cm-3,其摩尔质量为Mg・mol-1,则下列有关该晶体的说法正确的是(?)
g・cm-3,其摩尔质量为Mg・mol-1,则下列有关该晶体的说法正确的是(?)
| r+/r- | 配位数 | 实例 |
| 0.225~0.414 | 4 | ZnS |
| 0.414~0.732 | 6 | NaCl |
| 0.732~1.0 | 8 | CsCl |
| >1.0 | 12 | CsF |
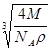 cm
cm参考答案:D
本题解析:AB晶体的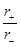 等于0.8,晶体结构类似于CsCl,每个晶胞中含有2个的A2+、2个B2-个数比应为1:1,所以A项、B项错误,D项正确;该晶体晶胞的边长为
等于0.8,晶体结构类似于CsCl,每个晶胞中含有2个的A2+、2个B2-个数比应为1:1,所以A项、B项错误,D项正确;该晶体晶胞的边长为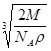 cm。
cm。
本题难度:一般
2、填空题 光健康、太阳能、绿色节能、零排放等高科技点亮2010上海世博。
(1)世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分解为无毒物质,汽车尾气中下列物质中属于由极性键构成的非极性分子为____。
A.CO2 B.NO C.NO2 D.CO
(2)“一轴四馆”中安装了高亮度节能的陶瓷金卤灯,金卤灯中填充物通常包含Na、81Tl、49In、Sc、I等元素的单质及化合物。有关说法正确的是____。
A.第ⅢA元素铊和铟,第一电离能T1大于In
B.元素Sc位于周期表d区
C.钠的熔点低,是因为金属键较弱
D.I2溶于KI溶液,可产生I3-,由价层互斥理论可推知I3-呈直线形
(3)“东方之冠”(中国馆)表面装有7000多块红色铝板,红色铝板为新型氟碳喷涂型材,一种氟碳涂层聚酯(FEP),它的单体为CF3-CF=CF2,该分子中碳原子的杂化方式有____。
(4)上海城区大规模集中使用“21世纪绿色光源”LED半导体照明,LED晶片采用砷化镓(GaAs)等材料组成。其中As原子在基态时外围电子排布式为:_____。GaAs的晶胞结构如图,晶胞中含镓原子数为____。 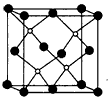
(5)世博馆广泛采用了冰蓄冷空调。冰蓄冷空调采用液态化合物乙二醇(HOCH2CH2OH)介质,乙二醇沸点高,是由于_______________________。
参考答案:(1)A
(2)BCD
(3)sp2、sp3
(4)4s24p3;4
(5)乙二醇分子间存在氢键
本题解析:
本题难度:一般
3、简答题 卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于周期表的______区;溴的价电子排布式为______.
(2)在不太稀的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是______.
(3)请根据表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是______.
| 氟 | 氯 | 溴 | 碘 | 铍 第一电离能 (kJ/mol) 1681 1251 1140 1008 900 |
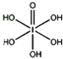 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6______HIO4.(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6______HIO4.(填“>”、“<”或“=”)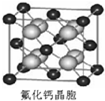
参考答案:(1)根据构造原理知,卤族元素最后填入的电子为p电子,所以卤族元素位于元素周期表的p区;溴是35号元素,最外层电子为其价电子,4s能级上排列2个电子,4p能级上排列5个电子,所以其价电子排布式为4s24p5,故答案为:p;4s24p5;
(2)HF分子之间存在氢键,使氢氟酸分子缔合,故答案为:氢键;
(3)卤族元素包含:F、Cl、Br、I、At元素,元素的第一电离能越小,元素失电子能力越强,得电子能力越弱,则越容易形成阳离子,根据表中数据知,卤族元素中第一电离能最小的是I元素,则碘元素易失电子生成简单阳离子,故答案为:I;
(4)H5IO6(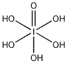 )中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,故答案为:<;
)中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,故答案为:<;
(5)离子晶体中离子电荷越多,半径越小离子键越强,离子晶体的晶格能越大,已知已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,所以发生的反应为CsICl2=CsCl+ICl,故答案为:A;
(6)ClO2-中心氯原子的价层电子对数n=2+7+1-2×22=4,属于sp3杂化;等电子体具有相同的电子数目和原子数目的微粒,所以与ClO2-互为等电子体的分子为Cl2O、OF2等,故答案为:sp3;Cl2O或OF2;
(7)该晶胞中含有钙离子个数=18×8+12×6=4,含有氟离子个数=8,近相邻的两个Ca2+的核间距为acm,则晶胞棱长=
本题解析:
本题难度:一般
4、选择题 已知BF3分子的空间构型为平面三角形,用等电子原理判断,下列分子或离子的立体构型不是平面三角形的是
[? ]
A.SO3
B.PCl3
C.NO3-
D.BCl3
参考答案:B
本题解析:
本题难度:简单
5、选择题 某晶体的一部分如图所示,这种晶体中A、B、C三种粒子数之比是 (?)。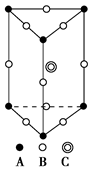
A.3∶9∶4?B.1∶4∶2
C.2∶9∶4?D.3∶8∶4
参考答案:B
本题解析:由图可知该晶体部分结构的上下两面为正三角形,因此处于顶点的粒子为12个晶胞共用,故A的数目为6×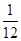 =
=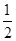 ;处于水平棱上的粒子为4个晶胞共用,处于垂直棱上的粒子为6个晶胞单元共用,故该结构单元中包含B粒子的数目为:6×
;处于水平棱上的粒子为4个晶胞共用,处于垂直棱上的粒子为6个晶胞单元共用,故该结构单元中包含B粒子的数目为:6×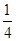 +3×
+3×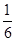 =2,由此可见A、B、C三种粒子的数目之比为
=2,由此可见A、B、C三种粒子的数目之比为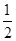 ∶2∶1=1∶4∶2。
∶2∶1=1∶4∶2。
本题难度:简单