时间:2017-08-22 16:45:33
1、选择题 下图中 4种装置①盛 100mLCuSO4,②盛200mL 0.01mol/ LH2SO4,③盛200mL ZnCl2,④盛200mL NaCl饱和溶液工作一段时间后,测得导线上均通过了0.002 mol电子,此时溶液的 pH值由大到小的排列顺序为(不考虑盐的水解和溶液体积变化)?
A.④②③①
B.④③①②
C.④③②①
D.④①③②
</PGN0015B.TXT/PGN>
参考答案:C
本题解析:4个装置①是电解CuSO4,生成H2SO4转移0.02mol电子,生成[H+]0.002/0.1=0.02(mol/L),②装置为原电池,在Cu板上有H2放出,2H++2e=H2↑转移0.002mol电子,则消耗0.002molH+,溶液中剩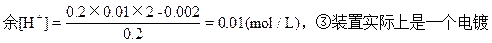
池,pH值不变,④装置为电解NaCl饱和溶液,生成NaOH,pH值最大,所以正确的顺序为:④③②①。
本题难度:一般
2、填空题 (18分)氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为: 。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____________.
。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____________.
a.电能全部转化为化学能
b. 的物质的量浓度不变(不考虑溶液体积变化)
的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液 白色沉淀
白色沉淀 观察现象并判断。则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是___________。
观察现象并判断。则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是___________。
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式__________。
(3)已知
 。某同学设想用下列流程得到BaCl2,
。某同学设想用下列流程得到BaCl2,
则①的离子方程式为_________,该反应的平衡常数K=__________;
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg・L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
I.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液,发生 反应
反应
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:
请回答:
①确定操作Ⅱ完全反应的现象是___________。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是__________。
参考答案:(1)2NH3-6e-+6OH-=N2+6H2O;bd。(2)①HCl;2SO2+2Ba2++O2+2H2O=2BaSO4+4H+,②SO2+2H2O-2e-=4H++2SO42-(3)BaSO4+CO32- BaCO3+SO42-0.04(4)①溶液蓝色褪去,②ClO2-+4I-+4H+=Cl-+2I2+2H2O(每空2分)
BaCO3+SO42-0.04(4)①溶液蓝色褪去,②ClO2-+4I-+4H+=Cl-+2I2+2H2O(每空2分)
本题解析:(1)氨气燃料电池中氨气中的氮元素化合价升高,在负极反应,所以负极的电极反应为:2NH3-6e-+6OH-=N2+6H2O;a电解装置不可能将电能全部转化为化学能,还有热能,错误;b硫酸根离子在电解精炼中没有反应,不变,正确;c铜离子向阴极移动,错误;d阳极上比铜活波的金属反应,比铜不活波的金属会作为阳极泥落下来,正确;e阳极是铝、锌等先反应,所以阳极质量减少了64克,不是铜减少了64克,不能计算转移电子数,错误。所以选bd。(2)①所得的悬浊液经过过滤得到白色沉淀,在加入盐酸看沉淀是否溶解,若未溶解,说明反应过程中二氧化硫被氧气氧化成了硫酸根离子,所以反应的离子方程式为:2SO2+2Ba2++O2+2H2O=2BaSO4+4H+。②若用电解法吸收尾气中的二氧化硫,则二氧化硫在阳极失去电子变成硫酸根离子,电极反应为:SO2+2H2O-2e-=4H++SO42-(3)因为Ksp(BaSO4)<Ksp(BaCO3),所以硫酸钡可以转变成碳酸钡,BaSO4(s)+CO32-(aqs)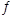 BaCO3(s)+SO42-(aq),其平衡常数等于Ksp(BaSO4)/<Ksp(BaCO3)=0.04。(4)①操作Ⅱ使碘单质反应,所以完全反应的现象为溶液蓝色褪去。②pH至1~3,溶液中的离子从ClO2-变成Cl-,氯元素的化合价降低,所以碘元素的化合价升高,从-1价的碘离子变成碘单质,溶液又显蓝色。ClO2-+4I-+4H+=Cl-+2I2+2H2O
BaCO3(s)+SO42-(aq),其平衡常数等于Ksp(BaSO4)/<Ksp(BaCO3)=0.04。(4)①操作Ⅱ使碘单质反应,所以完全反应的现象为溶液蓝色褪去。②pH至1~3,溶液中的离子从ClO2-变成Cl-,氯元素的化合价降低,所以碘元素的化合价升高,从-1价的碘离子变成碘单质,溶液又显蓝色。ClO2-+4I-+4H+=Cl-+2I2+2H2O
考点:电解精炼,难溶电解质的转化,氧化还原反应
本题难度:困难
3、选择题 电解含下列离子的水溶液,若阴极析出相等质量的金属,则消耗的电量最多的是
A.Ag +
B.Cu2+
C.Na+
D.Mg2+
参考答案:B
本题解析:既然是电解含有离子的水溶液,所以不可能析出钠单质、镁单质,因为在阴极氢离子得电子的能力比Na+ 、Mg2+得电子能力强,所以应该看A、B选项,假设都析出mg金属,Ag + 需要消耗的电量为m/108,Cu2+消耗的电量为2m/64,所以消耗电量最多的是Cu2+,故选B。
本题难度:一般
4、填空题 工业上利用含有一定浓度的I2和CuSO4溶液的工业废水制备饲料添加剂Ca(IO3)2,其生产流程如下:
已知:Ca(IO3)2微溶于水,溶于硝酸;Ksp(CuI)=1.1×10-12, Ksp(Cu2S)=2.5×10-48;
氧化性: HNO3>IO3―>H2O2
(1)“还原”过程中主要反应的化学方程式为:2Na2S2O3+I2 = + 2NaI。
(2)在还原过程还伴随有CuI生成,写出加入Na2S的离子反应方程式 。
(3)在氧化过程中先加入H2O2再加入浓硝酸,而不直接加入浓硝酸的目的是 。
(4)加入的石灰乳在溶液中反应而得到Ca(IO3)2,则要调节pH至 (填“酸性” 或“中性”或“碱性”),原因是 。
(5)Ca(IO3)2也可用电化学氧化法制取:先充分电解KI溶液,然后在电解后的溶液中加入CaCl2,最后过滤得到Ca(IO3)2。写出电解时阳极发生的电极反应方程式 ,用该方法制取Ca(IO3)2,每1kg碘化钾理论上可生产纯度为97.8%Ca(IO3)2的质量为 ____kg(计算结果保留3位有效数字)。
参考答案:(1) Na2S4O6 (2分)
(2)2CuI(s)+S2―=Cu2S(s)+2I― (3分)
(3)减少氧化过程中生成的氮的氧化物的污染 (2分)
(4)中性 (2分)Ca(IO3)2在硝酸溶液中溶解,故要中和过量的酸;在碱性溶液中,会混有微溶的Ca(OH)2造成产品不纯。 (2分)
(5)3H2O+I― -6e―=IO3―+6H+ (3分) ; 1.20(2分)
本题解析: (1)该过程称之为还原过程,可以肯定发生了氧化还原反应,所以根据方程式中的I的化合价降低可以知道,Na2S2O3 的中S的化合价升高,再根据Na、O原子守恒可以配平该方程式为2Na2S2O3+I2 = Na2S4O6+ 2NaI,还可以根据写出的化学方程式用电子得失配平验证。此处的难点关键在于缺项物质为中学阶段没接触过的连四硫酸钠,所以可能会出现想不到或是不敢写的情况,只要大胆利用所学的原则配平就可以了。
(2)还原过程中已经说明有沉淀CuI生成了,所以加入Na2S还会发生反应,则应该是通过已知条件中的沉淀溶解平衡常数进行比较得出结论,比较之下Cu2S比 CuI更加难溶,所以此时会发生沉淀转化,所以发生的反应方程式书写要按照沉淀溶解平衡的格式书写,方程式为2CuI(s)+S2―(aq)=Cu2S(s)+2I―(aq)。
(3)氧化步骤加入的H2O2 和浓硝酸起到氧化的目的,但是浓硝酸参与的反应容易产生氮氧化物污染环境,所以先加入过氧化氢。由于氧化性顺序HNO3>IO3―>H2O2 ,所以加入的过氧化氢只能把I-氧化为IO3- ,要使I2继续被氧化为IO3- ,还需要再加入浓硝酸,使浓硝酸反应更加完全,从而减少过程中氮氧化物的污染。
(4)加入石灰乳目的是反应得到Ca(IO3)2 ,且通过操作可以看出反应后要使Ca(IO3)2 尽可能多得以晶体形式析出,而Ca(IO3)2溶于硝酸,所以必须调节pH值把过量的硝酸中和掉,且加入的石灰乳不能过量,过量则会混入石灰乳沉淀杂质,所以应该调节pH至中性。
(5)用KI溶液电解制备Ca(IO3)2 溶液,则I-需要发生氧化反应在阳极放电生成IO3-,电解液是非碱性的,所以根据O原子守恒,IO3―中的O一定来源于H2O中,从而生成了H+,所以电极反应式为:3H2O+I― -6e―=IO3―+6H+ ;计算碘化钾的质量可以采用I原子守恒计算,所以有1/2n(KI)= n(Ca(IO3)2)=1000/166mol,m产品=M(Ca(IO3)2)×n(Ca(IO3)2)÷97.8%=390g/mol×1000/166mol÷97.8%≈1200g=1.20kg。
考点:本题考查的是化学工艺流程,涉及到了陌生的氧化还原反应缺项配平、沉淀转化、环境问题、PH调节、电化学基础、转化计算等内容。
本题难度:困难
5、选择题 下列对有关实验的描述不正确的是( )
A.在浓氨水中加入生石灰可以制取少量的NH3
B.用惰性电极电解熔融NaCl:2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.氯水和活性炭使红墨水褪色,能用同一原理解释
D.浓硫酸和浓盐酸长期暴露在空气中浓度都会降低
参考答案:BC
本题解析:A.生石灰可与水反应,并放出热量,氨气易挥发,可用于制备氨气,故A正确;B.电解熔融NaCl,生成钠和氯气,如电解氯化钠溶液,则生成氯气、氢气和氢氧化钠,故B错误;C.氯水具有强氧化性,而活性炭起到吸附作用,二者的原理不同,故C错误;D.浓硫酸具有吸水性,而盐酸易挥发,长期暴露在空气中浓度都会降低,故D正确,故选BC。
考点:考查氨气、氯气、电解以及浓硫酸的性质
本题难度:一般