时间:2017-08-22 15:16:56
1、填空题 (12分)铜和浓硫酸发生反应的化学方程式为: Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(1)浓H2SO4作_________剂,具有 性。
(2)在该反应中,若消耗了32 g Cu,则转移了_______mol 电子,还原了 mol H2SO4,生成 L SO2(标准状况)气体。
(3)以下三种物质的氧化性由强到弱的顺序为: (写出序号)
①浓H2SO4 ②稀H2SO4 ③CuSO4
参考答案:(1) 氧化剂 氧化性(2) 1 1 22.4 (3)①②③(每空2分)
本题解析:判断依据:升失氧,降得还;依方程式进行氧化还原反应的计算。
本题难度:一般
2、选择题 比较下列各组物质的沸点
①乙醇>丙烷 ②正戊烷>异戊烷 ③1-丁烯>1-庚烯,其中正确的是
A.①②
B.①③
C.②③
D.①②③
参考答案:A
本题解析:考查物质的物理性质。醇中存在分子间氢键,所以沸点高,①正确,烷烃同分异构体中支链越多,沸点越低,②正确。烯烃同系物中,碳原子树越低,沸点越高,③不正确。所以答案是A。
本题难度:简单
3、填空题 (4分)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的 Fe3+。这个变色的过程中的Fe2+被 (填“氧化”或“还原”)。若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有: (选择填空)。
A.氧化性
B.还原性
C.酸性
D.碱性
参考答案:氧化 B
本题解析: 亚铁离子变成铁离子,化合价升高,被氧化,加入维生素C,可以使铁离子变回亚铁离子,铁元素化合价降低,维生素的元素化合价升高,所以维生素表现了还原性。
考点:氧化还原反应。
本题难度:一般
4、填空题 A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如下图所示,其中Z元素原子最外层电子数是电子层数的2倍。请回答下列
问题: 
(1)W的最高价氧化物化学式是 ;Z的原子结构示意图为 。
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为 。
(3)AW3可用于净水,其原理是 。(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应。下列措施中既能提高
反应速率,又能提高原料转化率的是 。
a.升高温度
b.加入催化剂
c.将X的简单气态氢化物及时移离
d.增大反应体系的压强
(5)标准状况下,2.24L X的简单气态氢化物被200 mL l mol L-1X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示) 。
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成无毒气体而除去,写出用WY2(沸点9.9℃)氧化除去CN-的离子方程式 。
参考答案:(1)Cl2O7 
(2)Al(OH)3+NaOH=NaAlO2+2H2O
(3)Al3++3 H2O  Al(OH)3+3H+
Al(OH)3+3H+
(4)d
(5)NO3-、H+、NH4+、OH-
(6)2ClO2+2CN-=N2+2Cl-+2CO2
本题解析:
A是地壳中含量最多的金属元素,则A是Al;短周期中B的原子半径最大,B是Na;Z是最外层电子数是电子层的3倍,Z则是S,X、Y、W依次是N、O、Cl。
(1)W的最高价氧化物是Cl2O7;Z原子结构示意图为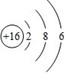 ;
;
(2)反应方程式为Al(OH)3+NaOH=NaAlO2+2H2O
(3)AlCl3净水原理是,Al3+发生水解,Al3++3 H2O  Al(OH)3+3H+ ;
Al(OH)3+3H+ ;
(4)提高转化率又能提高反应速率,选d。
(5)0.1mol NH3被0.2mol HNO3的溶液吸收后,是0.1molNH4NO3和0.1molHNO3组成的,由于NH4+能发生水解,离子浓度由大到小顺序为NO3-、H+、NH4+、OH-。
(6)2ClO2+2CN-=N2+2Cl-+2CO2
本题难度:困难
5、填空题 在中学化学中,常用作氧化剂的物质有 、 、 (列举出三种),常用作还原剂的物质有 、 、 (列举出三种)。
参考答案:氧化剂:氧气、氯气、浓硫酸、硝酸、高锰酸钾、氯化铁
还原剂:铝、锌、铁、碳、氢气、一氧化碳
本题解析:略
本题难度:简单