时间:2017-08-22 14:32:00
1、选择题 下列关于测定胆矾晶体里结晶水含量的实验操作,会引起测定结果偏高的是
A.加热时,强热蒸干,硫酸铜表面出现黑色固体
B.坩埚内附着有少量氯化钠固体
C.加热时,胆矾晶体未完全变白即停止加热
D.加热胆矾晶体后在空气中冷却称量
参考答案:A
本题解析:略
本题难度:简单
2、实验题 饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一。某兴趣小组进行了如下实验探究。
实验一:定性研究。
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色退去;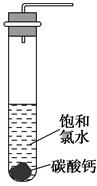
②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
第三份滤液加热,看到滤液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性比氯水强的原因是?。
(2)依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有?(填写溶质的化学式)。
实验二:定量研究。
在圆底烧瓶底部,用一塑料网包住块状石灰石(过量)与150 mL饱和氯水反应,按下图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,将装置密封后再加热,煮沸烧瓶中的液体,量筒中的气体不再增加时停止实验。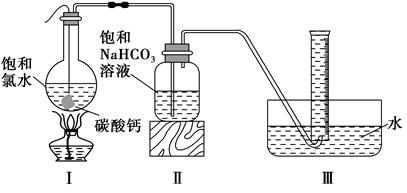
请回答:
(3)实验结束后检测到量筒中收集到的气体除CO2外还有O2,请写出Ⅰ中产生O2的化学反应方程式?。
(4)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,请你对装置Ⅲ进行改进(水槽中仍为水),最简单的方法是?。
参考答案:(1)CaCO3消耗了氯水中的盐酸,使可逆反应Cl2+H2O HCl+HClO的平衡向右移动,HClO浓度增大
HCl+HClO的平衡向右移动,HClO浓度增大
(2)Ca(HCO3)2
(3)2HClO 2HCl+O2↑
2HCl+O2↑
(4)将水槽中的水换为热水(答案合理即可)
本题解析:(1)由于次氯酸的酸性弱于碳酸的酸性,但强于HCO3-的酸性,所以碳酸钙只与盐酸反应,与氯水中的次氯酸是不反应的。即CaCO3消耗了氯水中的盐酸,使可逆反应Cl2+H2O HCl+HClO的平衡向右移动,HClO浓度增大,所以漂白性增强。
HCl+HClO的平衡向右移动,HClO浓度增大,所以漂白性增强。
(2)第一份滤液与石灰水混合,立即产生大量白色沉淀,第二份与稀盐酸混合,立即产生大量CO2,因此可以判断白色沉淀是碳酸钙,所以滤液中还存在的溶质是碳酸氢钙。
(3)次氯酸不稳定,受热易分解生成氧气和氯化氢,反应方程式为2HClO 2HCl+O2↑。
2HCl+O2↑。
(4)气体的溶解度随温度的升高而降低,所以要减小CO2溶解带来的损耗,可以将水槽中的水换为热水。
本题难度:一般
3、实验题 “碘钟”实验中,3I-+S2O82-=I3-+?2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
回答下列问题:
(1)该实验的目的是____________。
(2)显色时间t1=____________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为?__________(填字母)。
A.<22.0s?B.22.0~44.0s?C.>44.0s?D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是________________。?
参考答案:(1)研究反应物I-与S2O82-的浓度对反应速率的影响
(2)29.3s?
(3)A?
(4)化学反应速率与反应物起始浓度乘积成正比(或显色时间与反应物起始浓度乘积成反比)
本题解析:
本题难度:一般
4、简答题 实验室用加热1-丁醇、溴化钠和浓H2SO4的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成.反应结束后将反应混合物蒸馏,分离得到1-溴丁烷,已知相关有机物的性质如下:
| ? | ?熔点/℃ | ?沸点/℃ ?1-丁醇 -89.53 ?117.25 ?1-溴丁烷 -112.4 ?101.6 ?丁醚 -95.3 ?142.4 ?1-丁烯 -185.3 -6.5 |
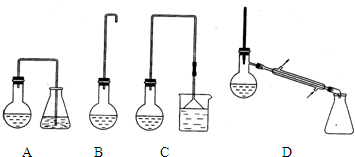
参考答案:(1)实验室用加热1-丁醇、溴化钠和浓H2SO4的混合物的方法来制备1-溴丁烷时,发生反应生成产物中含有易溶于水的溴化氢,还会有烯、醚等副产物生成,吸收装置需要防倒吸;制备1-溴丁烷的装置应选用上图中C;1-溴丁烷沸点101.6,反应加热时的温度不宜超过100℃,防止1-溴丁烷因气化而逸出,影响产率;
故答案为:C;防止1-溴丁烷因气化而逸出,影响产率;
(2)a.浓硫酸和1-丁醇反应发生副反应消去反应生成烯烃、分子间脱水反应生成醚,稀释后不能发生类似反应减少副产物烯和醚的生成,故a正确;
b.浓硫酸具有强氧化性嫩氧化溴离子为溴单质,稀释后减少Br2的生成,故b正确;
c.反应需要溴化氢和1-丁醇反应,浓硫酸溶解溶液温度升高,使溴化氢挥发,稀释后减少HBr的挥发,故c正确;
d.水不是反应的催化剂,故d错误;
故答案为:abc;
(3)反应结束后将反应混合物蒸馏,分离得到1-溴丁烷,应选用的装置为D,体积图表数据温度应控制在101.6℃≤t<117.25℃;
故答案为:D;101.6℃≤t<117.25℃;
(4)欲除去溴代烷中的少量杂质Br2,
a.NaI和溴单质反应,但生成的碘单质会混入,故a不选;
b.溴单质和氢氧化钠反应,溴代烷也和NaOH溶液中水解反应,故b不选;?
c.溴单质和NaHSO3 溶液发生氧化还原反应可以除去溴单质,故c选;
d.KCl不能除去溴单质,故d不选;
故答案为:c.
本题解析:
本题难度:一般
5、选择题 以下实验或操作不能达到目的的是
A.用铜片(必要时可加热)鉴别浓硝酸、稀硝酸、浓硫酸和浓盐酸
B.用品红溶液鉴别乙醛、苯、硝基苯
C.用10mL量筒准确量取8.00mL1mol/L的KMnO4溶液
D.用核磁共振氢谱图鉴别乙醇和甲醚
参考答案:
C
本题解析:
本题考查基本实验操作。量筒只能精确到0.1mL,C选项错误。
本题难度:一般