时间:2017-08-22 14:29:27
1、选择题 在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需要117 kJ ・mol-1~125 kJ ・mol-1 的热量,但1,3-环己二烯失去2个氢原子形成苯是放热反应,反应热是23.4 kJ ・mol-1 ,这表明
A.苯比1,3-环己二烯稳定
B.苯加氢生成环己烷是吸热反应
C.1,3-环己二烯比环己烷稳定
D.1,3-环己二烯加氢是吸热反应
参考答案:A
本题解析:A、1,3-环已二烯失去两个氢原子变成苯是放热反应,说明1,3-环已二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故A正确;
D、根据题意信息:烃分子中去掉两个氢原子形成一个双键是吸热反应,所以1,3-环已二烯加上两个氢原子是放热反应,故D错误;
B、根据题意信息可知,烃分子中去掉两个氢原子形成一个双键是吸热反应,所以烃分子中一个双键加上两个氢原子是放热反应,故B错误;
C、1,3-环已二烯失去两个氢原子变成苯是放热反应,说明1,3-环已二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故C错误。
故选A。
考点:吸热反应和放热反应 化学能与热能的相互转化
点评:本题考查学生吸热反应和放热反应的有关知识,可以根据所学知识来回答,难度不大。
本题难度:简单
2、选择题 下列反应属于吸热反应的是 ( )
A.碳在氧气中的燃烧
B.葡萄糖在人体内氧化分解
C.Ba(OH)2・8H2O与NH4Cl反应
D.锌粒与稀H2SO4反应制取H2
参考答案:C
本题解析:略
本题难度:简单
3、计算题 PM2.5(可入肺颗粒物)污染跟冬季燃煤密切相关,燃煤还同时排放大量的CO2、SO2和NOx
(1)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。
①已知在常温常压下:
2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g)?H = -1275.6 kJ/mol
2CO(g)+O2(g)=2CO2(g)?H = -566.0 kJ/mol?
H2O(g)=H2O(1)?H = -44.0 kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____________________。
②以甲醇和氧气反应制成的燃料电池如图所示,该电池工作过程中O2应从______(填“c”或“b”)口通入,电池负极反应式为__________________。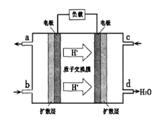
③25℃时,将甲醇燃烧生成的足量CO2通入到浓度为0.lmol・L-1,NaOH溶液中,所得溶液的pH=8,溶液中离子浓度由大到小的顺序是_________________。
(2)已知在一定条件下,NO与NO2存在下列反应:NO(g)+NO2(g)=N2O3(g),ΔH<0若该反应在绝热、恒容的密闭体系中进行,下列示意图能说明tl时刻达到平衡状态的是____________。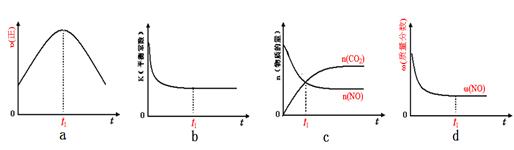
(3)在一个固定容积为5L的密闭容器中充入0.20molSO2和0.l0molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=__________,若继续通入0.20mo1SO2和0.lmolO2,则平衡____________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(4)在一定条件下,NO2可以被NH3还原为N2来消除NO2对环境造成的污染。25℃时,将NH3溶于水得l00mL 0.lmol・L-的氨水,测得pH=11,则该条件下NH3・H2O的电离平衡常数约为___________。
参考答案:(16分)
(1)?①CH3OH(l)+O2(g)=CO(g)+2H2O(l)?△H=-442.8kJ・mol-1(2分);
②c (2分)? CH3OH+ H2O-6e-=CO2↑+6H+(2分);
③c(Na+)> c(HCO- 3)> c(OH-)> c(H+)> c(CO2- 3) (2分);
(2)? bd (2分)
(3)? 0.036mol・L-1・min-1或0.0006mol・L-1・s-1(2分);向正反应方向(2分);
(4)? 1.01×10-5(2分)
本题解析:
(1)①根据盖斯定律①-②-③×4得到CH3OH(l)+O2(g)=CO(g)+2H2O(l)?△H=-442.8kJ・mol-1。②结合图像电池中质子移向正极,O2在正极反应。应从c通入,发生O2+4e-+4H+=2H2O,所以负极为CH3OH+ H2O-6e-=CO2↑+6H+。③溶液的pH=8应为溶质为碳酸氢钠,离子浓度由大到小的顺序是c(Na+)> c(HCO- 3)> c(OH-)> c(H+)> c(CO2- 3)。
(2)达到平衡状态时v(正)=v(逆),各物质的量不再改变,a、v(正)应该不在改变,错误。B、各物质的量不再改变,不再有能量变化,温度不变平衡常数不变,正确。c、各物质的量不再改变,错误。可知d、各物质的量不再改变,质量分数不变,正确。
(3)SO30.18mol,则转化的O2为0.09mol,v(O2)=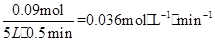 。
。
(4)NH3・H2O的电离平衡常数约为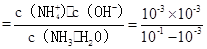 = 1.01×10-5。
= 1.01×10-5。
本题难度:一般
4、选择题 下列变化过程中,必需加入氧化剂才能实现的是
A.Na2O2→NaOH
B.CO2→CO
C.Fe2+→Fe3+
D.Ba(OH)2→BaSO4
参考答案:C
本题解析:分析:必需加入氧化剂才能实现,则选项中的物质为还原剂的变化,还原剂中元素的化合价升高,以此来解答.
解答:A.Na2O2→NaOH中O元素的化合价降低,发生氧化还原反应,但不需加还原剂,与水反应即可实现,故A不选;
B.CO2→CO中C元素的化合价降低,则需加还原剂才能实现,故B不选;
C.Fe2+→Fe3+中Fe元素的化合价升高,则需加氧化剂才能实现,故C选;
D.Ba(OH)2→BaSO4中元素的化合价没有变化,发生酸碱中和反应即可实现,故D不选;
故选C.
点评:本题考查氧化还原反应,明确元素的化合价变化是解答本题的关键,并注意氧化剂、还原剂中元素的变化来解答,难度不大.
本题难度:一般
5、填空题 下表是一些键能的数据(单位:KJ・mol-1)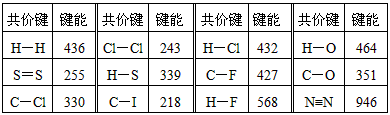
回答下列问题:
(1)H-H的键能为436 kJ/mol它所表示的意义是___________________
(2)一个化学反应的反应热(设反应物、生成物均为气态)与反应物和生成物中的键能之间有密切的关系。由表中数据计算下列热化学方程式中的热效应:H2(g)+Cl2(g) = 2HCl(g);△H=____________。
(3)共价键的极性强弱对化学反应有很大的影响。卤代烃RX在同样条件下发生碱性水解反应时
(RX+NaOH → R-OH+NaX),则RF、RCl、RBr、RI(R相同)的反应活性由大到小的顺序是___________________。
(4)试预测C-Br键的键能范围(写具体数值)_______< C-Br键能<_________。
参考答案:(1)“略”
(2)-185kJ・mol-1
(3)RF<RCl<RBr<RI
(4)218kJ・mol-1;330kJ・mol-1
本题解析:
本题难度:一般