时间:2017-08-10 02:44:20
1、选择题 将足量AgCl分别放入下列物质中,AgCl的溶解度由大到小排列顺序是( )
①20mL?0.01mol?L-1KCl溶液?
②30mL?0.02mol?L-1CaCl2溶液
③40mL?0.03mol?L-1?HCl溶液?
④10mL蒸馏水
⑤50mL?0.05mol?L-1?AgNO3溶液.
A.①>②>③>④>⑤
B.④>③>⑤>②>①
C.⑤>④>②>①>③
D.④>①>③>②>⑤
参考答案:根据c(Ag+)或c(Cl-)大小比较,c(Ag+)或c(Cl-)越小,AgCl的溶解度越大,
①c(Cl-)=0.01mol/L,②c(Cl-)=0.04mol/L,③c(Cl-)=0.03mol/L,④c(Ag+)或c(Cl-)为0,⑤c(Ag+)=0.05mol/L,
则AgCl的溶解度由大到小排列顺序是④>①>③>②>⑤,
故选D.
本题解析:
本题难度:简单
2、选择题 25℃时,已知下列三种金属硫化物的溶度积常数(Ksp)分别为:Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24.下列关于常温时的有关叙述正确的是( )
A.硫化锌、硫化铜、硫化亚铁的溶解度依次增大
B.将足量的ZnSO4晶体加入到0.1mol/L的Na2S溶液中,Zn2+的浓度最大只能达到1.6×10-23mol/L
C.除去工业废水中含有的Cu2+,可采用固体FeS作为沉淀剂
D.向饱和的FeS溶液中加入FeSO4溶液后,混合液中c(Fe2+)变大、c(S2-)变小、但Ksp(FeS)变大
参考答案:解;A、由于Ksp(CuS)=1.3×10-36<Ksp(ZnS)=1.6×10-24<Ksp(FeS)=6.3×10-18,所以溶解度CuS<ZnS<FeS,故A错误;
B、原硫化钠溶液中硫离子增大浓度为:c(S2-)=0.1 mol/L,所以锌离子最小浓度为:c(Zn2+)=1.6×10240.1mol/L=1.6×10-2 3mol/L,故B错误;
C、由于Ksp(CuS)=1.3×10-36<Ksp(FeS)=6.3×10-18,硫化铜的溶解度小于硫化亚铁的,所以除去工业废水中含有的Cu2+,可采用FeS 固体作为沉淀剂,故C正确;
D、向饱和的FeS 溶液中加入FeSO4溶液后,混合液中c(Fe2+)变大、c(S2-)变小,温度不变,所以Ksp(FeS)不变,故D错误;
故选:C.
本题解析:
本题难度:一般
3、选择题 常温时,将足量的AgCl固体分别加入同体积的下列各溶液中,溶解的AgCl最少的是( )。
A.1 mol・L-1的MgCl2溶液
B.2 mol・L-1的NaCl溶液
C.1.4 mol・L-1的BaCl2溶液
D.1 mol・L-1的AlCl3溶液
参考答案:D
本题解析:略
本题难度:简单
4、选择题 已知AgCl能溶于氨水而生成[Ag(NH3)2]+.NH4Cl溶液和AgNO3溶液混合后,再滴入NaOH溶液,溶液中沉淀量y与NaOH溶液加入量x的关系曲线不可能是( )
A.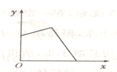
B.
C.
D.
参考答案:分析时应注意考虑到NH4Cl溶液和AgNO3溶液混合后,二者是否能恰好反应完,若不能,AgNO3是否过量,因为Ag+在碱性条件下可生成AgOH沉淀.
A、若AgNO3过量,加入NaOH后,开始时沉淀量增加,后来因有一部分AgCl沉淀转化为[Ag(NH3)2]+而减少,因NH4+的量不足,故沉淀不可能全部转化为[Ag(NH3)2]+,故A错误;
B、若AgNO3过量,加入NaOH后,开始时沉淀量增加,后来因有一部分AgCl沉淀转化为[Ag(NH3)2]+而减少,因NH4+的量不足,故沉淀不可能全部转化为[Ag(NH3)2]+,故B正确;
C、若混合前n(NH4Cl)≥2n(AgNO3),加入足量NaOH后沉淀全部溶解,故C正确;
D、若2n(AgNO3)>n(NH4Cl)>n(AgNO3),加入一定量NaOH溶液,沉淀部分溶解,故D正确;
故选A.
本题解析:
本题难度:简单
5、简答题 2011年8月12日,《云南信息报》首度披露?了云南曲靖铬污染事件,引起全国广泛关注.工业上将制取重铬酸钾(K2Cr2O7)和铬酸酐(CrO3)的剩余废渣称为铬渣,其成分为:SiO2、Al2O3、MgO、Fe2O3、CrO3、K2Cr2O7等.
已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小.
③下表为一些金属氢氧化物沉淀的pH参照数据.
| 物质 | ?开始沉淀 | ?完全沉淀 ?Fe(OH)3 ?2.7 ?3.7 ?Al(OH)3 ?3.7 ?4.7 ?Cr(OH)3 ?4.7 ?a ?Fe(OH)2 ?7.6 ?9.6 ?Mg(OH)2 ?9.6 ?11.1 |
参考答案:(1)根据污水中物质的含量可知,加入硫酸后,除SiO2不溶过滤除去外,其他金属离子均生成其简单阳离子,且Cr为+6价,根据题意可知有毒,需要被还原为+3价,
故答案为:将高价有毒的+6Cr元素含有成无毒的+3Cr;
(2)结合沉淀的pH,溶液由强酸性到4.7,只有Fe(OH)3和Al(OH)3生成.KspCr(OH)3=c(Cr3+)×c3(OH-),若c(Cr3+)=10-5mol/L时,c(OH-)=310-3210-5
本题解析:
本题难度:一般