时间:2017-08-10 02:15:04
1、选择题 为中国近代化学发展做出突出贡献的科学家是
A.李四光
B.华罗更
C.候德榜
D.钱学森
参考答案:B
本题解析:题述四个选项中的科学家均为我国科学事业的发展做出了突出的贡献。其中,李四光是我国当代著名的地质学家;华罗更是著名的数学家;钱学森是著名的物理学家;候德榜被称为中国近代化学史上的第一颗明星,为中国化学工业发展做出卓越贡献,是中国近代化工工业的奠基人,他发明的联合制碱法为中华民族争得了荣誉。
本题难度:简单
2、填空题 工业上常用氟磷灰石[Ca5(PO4)3F]为原料,按如下图所示流程制取磷酸、重过磷酸钙[Ca(H2PO4)2]和氢氟酸。图中反应(Ⅰ)为氟磷灰石跟另一种原料反应,生成A、B、C三种物质,其中的产物C又跟氟磷灰石发生反应(Ⅱ),生成B和重过磷酸钙。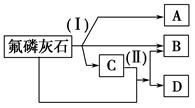
试写出两个反应的化学方程式:反应(Ⅰ)______________;反应(Ⅱ)___ _______
在生产中要特别注意_____________________________________________
参考答案:(Ⅰ)Ca5(PO4)3F+5H2SO4=3H3PO4+5CaSO4+HF↑
(Ⅱ)Ca5(PO4)3F+7H3PO4=5Ca(H2PO4)2+HF↑ 由于HF有毒,因而生产中要特别注意加强劳动保护和防止环境污染
本题解析:解题时,可以把Ca5(PO4)3F看成是Ca3(PO4)2和CaF2的固定组成物,由Ca3(PO4)2、CaF2与浓硫酸的反应化学方程式不难类推出Ca5(PO4)3F与硫酸的反应化学方程式。
本题难度:一般
3、选择题 工业生产的生石灰中常混有二氧化硅和石灰石。现将该生石灰样品溶于过量的盐酸中。然后在不断搅拌(必要时可以加热)的情况下,向反应混合液中逐滴加入氢氧化钠溶液至过量,如果纵坐标表示固体难溶物的质量(m),横坐标表示所加入氢氧化钠溶液的体积(V),则下列图示正确的是( )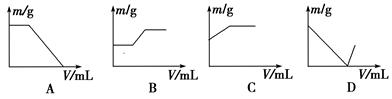
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列不需要用到二氧化硅的是
A.光导纤维
B.计算机芯片
C.石英钟表
D.玛瑙手镯
参考答案:B
本题解析:略
本题难度:一般
5、填空题 [化学――选修化学与技术](15分)
硫酸工业生产应考虑综合经济效益问题。
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在?的郊区(填选项的标号)
A.有丰富黄铁矿资源的城市
B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市
D.人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1t 98%硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应:SO2(g)+1/2O2(g)=SO3(g);△H=-98.3kJ・mol-1;放出的热量能在生产过程中得到充分利用,则每生产1t98%硫酸只需外界提供(或可向外界输出)?千焦能量;
(3)CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为??。
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 矿渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
参考答案:(1)C?(3分)
(2)输出6.23×105kJ能量?(4分)
(3)4CuFeS2+13O2=4CuO+2Fe2O3+8SO2?(4分)
(4)SO2转化为SO3是正反应放热的可逆反应,随温度升高,平衡逆移,SO3物质的量减少,所以CuSO 4的量减少(或温度升高,SO3物质的量减少,故CuSO4的量减少)(4分)
4的量减少(或温度升高,SO3物质的量减少,故CuSO4的量减少)(4分)
本题解析:略
本题难度:一般