时间:2017-08-10 01:54:02
1、选择题 在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是
[? ]
①滴有石蕊的NH4Cl溶液
②滴有石蕊的CO2溶液
③滴有石蕊的H2SO4溶液
④滴有酚酞的氨水溶液
⑤滴有酚酞的氢氧化钠溶液
⑥滴有酚酞的饱和氢氧化钙溶液
⑦滴有酚酞的Na2CO3溶液
⑧ 溶有SO2的品红溶液
A.②④
B.①③⑤⑦
C.①④⑥⑧
D.②④⑥
参考答案:D
本题解析:
本题难度:一般
2、选择题 在蒸发皿中加热蒸干下列物质的溶液并灼烧,可得原有物质的固体是( ? )
A.氯化铝
B.碳酸氢镁
C.硫酸亚铁
D.碳酸钠
参考答案:D
本题解析:
本题难度:简单
3、选择题 物质的量浓度相同的下列溶液,pH由大到小排列正确的是
[? ]
A.Ba(OH)2、Na2SO3、FeCl3、KCl
B.Na2SiO3、Na2CO3、KNO3、NH4Cl
C.NH3・H2O、H3PO4、Na2SO4、H2SO4
D.NaHCO3、C6H5COOH、C2H5OH、HCl
参考答案:B
本题解析:
本题难度:一般
4、填空题 某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B===H++HB-? HB-?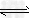 H++B2-?
H++B2-?
回答下列问题:
(1)Na2B溶液显________(填“酸性”“中性”或“碱性”),理由是_____________________。(用离子方程式表示)
(2)在0.1?mol・L-1?Na2B溶液中,下列粒子浓度关系式正确的是________。
A.c(Na+)+(OH-)=c(H+)+c(HB-)
B.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-)
C.c(Na+)=2c(B2-)+2c(HB-)
(3)已知0.1?mol・L-1?NaHB溶液的pH=2,则0.1mol・L-1?H2B溶液中氢离子的物质的量浓度可能是________?0.11?mol・L-1(填“<”“>”或”=”),理由是_____________________。
(4)0.1?mol・L-1?NaHB溶液中各种离子浓度由大到小的顺序是_______________。
参考答案:(1)碱性 ;B2- +H2O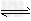 HB-+OH-?
HB-+OH-?
(2)BC
(3)< ;第一步电离产生的H+抑制了HB-的电离
(4)c(Na+)>c(HB-)>c(H+)>c(B2-)>c(OH-)
本题解析:
本题难度:一般
5、选择题 下列各溶液中微粒的物质的量浓度关系不正确的是( )
A.10?mL?1?mol?L-1?NH4?C1溶液与5mL?0.2mol?L-1Na?OH溶液混合?c(Na+)=c(Cl-)>c(OH-)>c(H+)
B.0.1mol?L-1Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S)
C.只含有Na+、H+、Cl-、OH-的溶液中一定有:c(Cl-)=c(Na+)>c(H+)=c(OH-)
D.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3和NH4?C1三种溶液中:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4?C1)
参考答案:A、10?mL?1?mol?L-1?NH4?C1溶液与5mL?0.2mol?L-1Na?OH溶液混合后,恰好发生反应生成氯化钠和氨水,溶液显示碱性,c(OH-)>c(H+),氯化钠完全电离,所以c(Na+)=c(Cl-)>c(OH-)>c(H+),故A正确;
B、硫化钠溶液中存在质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H2S),故B正确;
C、只含有Na+、H+、Cl-、OH-的溶液中的溶质的可能组成情况有:氯化钠和盐酸的混合物,c(Cl-)>c(Na+)>c(H+)>c(OH-);或者是氯化钠的水溶液,此时c(Na+)=c(Cl-)>c(OH-)=c(H+),还可以是氯化钠和氢氧化钠的混合物,此时c(Na+)>>c(OH-)>c(Cl-)>c(H+)等情况,故C错误;
D、(NH4)2SO4、(NH4)2CO3和NH4?C1三种溶液中,铵根离子的水解程度依次是:无影响、受促进,无影响,(NH4)2SO4、(NH4)2CO3中铵根离子浓度一定是大于等浓度的氯化铵中铵根离子浓度,即等浓度的三种溶液中,铵根离子浓度关系是(NH4)2SO4、>(NH4)2CO3>NH4?C1,当铵根离子浓度相等时,则c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4?C1),故D正确.
故选C.
本题解析:
本题难度:简单