时间:2017-08-10 01:46:29
1、选择题 下列化学用语书写不正确的是( )
A.氯离子的结构示意图: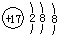
B.乙烯的结构简式:CH2=CH2
C.氯化镁的电子式: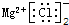
D.苯的化学式:C6H6
参考答案:A.氯原子得1个电子形成氯离子,氯离子核外电子数为18,核外有3个电子层,由里到外各层电子数为2、8、8,氯离子结构示意图为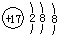 ,故A正确,;
,故A正确,;
B.乙烯分子式为C2H4,碳原子之间形成2对共用电子对,氢原子与碳原子之间形成1对共用电子对,乙烯的结构简式:CH2=CH2,故B正确;
C.氯化镁电子式中2个氯离子不能合并书写,氯化镁的电子式为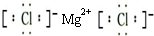 ,故C错误;
,故C错误;
D.苯分子中含有6个碳原子、6个H原子,烃中氢原子书写在后边,苯的化学式为C6H6,故D正确;
故选C.
本题解析:
本题难度:一般
2、填空题 (1)下列曲线表示卤素元素某种性质随核电荷数的变化趋势,正确的是____________。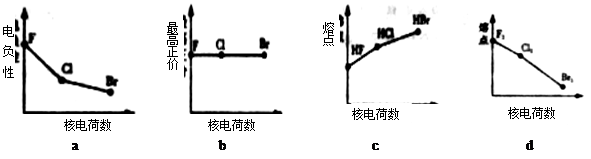
(2)利用“卤化硼法”合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为________,该功能陶瓷的化学式为___________。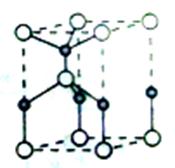
(3)BCl3和NCl3中心原子的杂化方式分别为________和_________。第一电离能介于B、N之间的第二周期元素有________种。
(4)若BCl3与XYm通过B原子与X原子间的配位健结合形成配合物,则该配合物中提供孤对电子的原子是________。
(5)SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O・CaO・6SiO2。
长石是金属铝硅盐。由钠长石化学式NaAlSi3O8可推知钙长石改写成氧化物的形式可表示为 ?
参考答案:
(1)a?(2)2;BN?(3)sp2;sp3? ;3(4)X?(5)CaO.Al2O3.6SiO2
本题解析:(1)随着核电荷数的增加,卤素元素得电子能力减弱,电负性逐渐减弱;a正确,氟元素没有正价,b错误,对应氢化物HF分子间有氢键存在,熔点最高,c错误,单质的熔点,取决于分子间作用力,结构相似,相对分子质量越大,分子间作用力越强,熔点越高,d错误。(2)利用“卤化硼法”合成含B和N两种元素的功能陶瓷,B和N两种元素在同一周期,原子半径逐渐减小,B大于N,因此白球是B,黑球是N,根据晶胞图,B在8个顶点和体心一个,因此8个顶点分摊后8乘八分之一,只有一个,加上体心一个共有2个,N在棱上有4个和体心一个,棱上4个分摊后4乘四分之一,只有一个,加上体心一个共有2个,所以化学式BN,(3)BCl中的B原子的杂化方式类似BF3属于sp2杂化;NCl3中的N原子的杂化方式类似NH3属于sp3杂化。根据电离能的变化规律,半充满的N原子和全充满的Be原子第一电离能属于特殊情况,要比同周期原子序数大的原子高,故第一电离能介于B、N之间的第二周期元素有Be、C、O三种元素。(4) BCl3是缺电子化合物,B原子的所有价电子已经使用,因而提供孤对电子的原子是X。(5)由钠长石化学式NaAlSi3O8可推知钙长石化学式CaAlSi6O16改写成氧化物的形式可表示为CaO.Al2O3.6SiO2
本题难度:一般
3、选择题 下列说法中不正确的是( )
A.在共价化合物中不可能含有离子键
B.含有共价键的化合物不一定是共价化合物
C.主族元素形成的阴离子不一定都满足8电子结构
D.非金属之间形成的化学键一定是共价键
参考答案:D
本题解析:
本题难度:简单
4、选择题 与主族元素在元素周期表中所处的位置有关的是( )
A.相对原子质量
B.核内中子数
C.次外层电子数
D.电子层数和最外层电子数
参考答案:元素核外电子层数等于周期表的周期数,元素的最外层电子数等于主族元素的序数,原子的核外电子排布决定元素在周期表中的位置.
故选D.
本题解析:
本题难度:一般
5、选择题 下列各数值表示有关元素的原子序数,它们所表示的各组原子中,能以共价键相互结合形成稳定化合物的是( )
A.11与9
B.17与17
C.16与8
D.2与8
参考答案:C
本题解析:
本题难度:简单