时间:2017-08-10 01:06:17
1、选择题 下列物质中不能发生水解反应的是( )
A.乙酸乙酯
B.淀粉
C.蛋白质
D.果糖
参考答案:D
本题解析:果糖是单糖,不能水解。A是酯类,可以水解,淀粉是多糖,也可以水解。蛋白质水解得到各种氨基酸。所以正确的答案是D。
本题难度:一般
2、选择题 下列叙述不正确的是
A.在0.1 mol/LCH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
B.在0.1 mol/L某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.CH3COOH和CH3COONa的混合溶液中,若c(CH3COO-)大于c(Na+),则溶液显酸性
D.10 mL0.02 mol/LHCl溶液与10 mL0.02 mol/LBa(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
参考答案:B
本题解析:
本题难度:困难
3、填空题 (共8分)A、B、C、D、E均为可溶于水的固体,组成他们的离子有
| 阳离子 | Na+ Mg2+ Al3+ Ba2+ |
| 阴离子 | OH- Cl- CO32- SO42- HSO4- |
参考答案:(1)Na2CO3、Al2(SO4)3、MgCl2、Ba(OH)2、NaHSO4[或Mg(HSO4)2]
(2)2Al3++3SO42- +3Ba2+ +8OH-=== 3BaSO4↓+2AlO2- +4H2O
(3)c( Na+)> c(CO32-)>c( OH-) >c(HCO3-)>c( H+)
本题解析:阴离子CO32-只能和Na+结合为Na2CO3;OH-能和Ba2+结合为溶于水的Ba(OH)2,则SO42-和Al3+结合成的物质为Al2(SO4)3;最后剩余Cl-和HSO4-结合的阳离子Na+、Mg2+;由题干可知A和B、C、D都生成沉淀且沉淀都溶于酸溶液,所以A为Na2CO3;E中含HSO4-,沉淀可以是Mg2+、Al3+、Ba2+的碳酸盐沉淀;B、C、D物质中分别含这三种阳离子,由④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失,说明溶解的沉淀是Al(OH)3,可推出B为Al2(SO4)3,D为Ba(OH)2,C为MgCl2,符合①②③沉淀形成的性质;①②生成的沉淀溶解于E,说明E中不能含和硫酸根离子、镁离子生成沉淀的离子,则E只能为:NaHSO4(或Mg(HSO4) 2),(1)综上所述,A为Na2CO3,B为Al2(SO4)3,C为MgCl2,D为Ba(OH)2,E为NaHSO4[或Mg(HSO4)2];(2)④中反应的离子方程式为2Al3++3SO42- +3Ba2+ +8OH-=== 3BaSO4↓+2AlO2- +4H2O;(3)A为碳酸钠,碳酸根离子水解显碱性,第一步水解大于第二步水解,则离子浓度大小为c( Na+)> c(CO32-)>c( OH-) >c(HCO3-)>c( H+)。
考点:考查无机物的推断。
本题难度:困难
4、填空题 常温下,0.1m01/L的下列溶液:
①HCl、②CH3COOH、③CH3COONa、④NaOH、⑤FeCl3、⑥NaCl。
(1)pH由小到大排列顺序为 (填序号);
(2)实验室配制⑤的溶液时常需加入少量盐酸,否则得到的是浑浊的溶液,产生浑浊的原因是(用离子方程式表示)
(3)物质的量浓度相同的①氨水②氯化铵③碳酸氢铵④硫酸氢铵⑤硫酸铵
在上述五种溶液中,铵根离子物质的量浓度由大到小的顺序是
(4)已知拆开1molH―H键,1molN―H键,1molN≡N键分别需要的能量是436kJ、39l kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为
参考答案:(1)①②⑤⑥③④ (2)Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
(3)⑤>④>②>③>① (4)N2(g)+3H2(g) 2NH3(g)
2NH3(g) 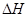 =-92.0kJ/mol
=-92.0kJ/mol
本题解析:(1)盐酸是一元强酸,醋酸是一元弱酸,醋酸钠是弱酸强碱盐,氢氧化钠是一元强碱。氯化铁是强酸弱碱盐,氯化钠是强酸强碱盐,所以在浓度相等的条件下,pH由小到大排列顺序为①②⑤⑥③④。
(2)氯化铁溶于水,铁离子水解生成氢氧化铁和盐酸,所以加入盐酸的目的是抑制铁离子的水解,方程式是Fe3++3H2O Fe(OH)3+3H+。
Fe(OH)3+3H+。
(3)在溶液中NH4+水解,而硫酸氢铵能电离出氢离子,抑制NH4+水解。HCO3-水解,显碱性,促进NH4+水解,所以五种溶液中,铵根离子物质的量浓度由大到小的顺序是⑤>④>②>③>①。
(4)反应热是断键吸收的能量和形成化学键所放出的能量的差值,则该反应的反应热△H=3×436kJ/mol+946kJ/mol-2×3×391kJ/mol=-92.0kJ/mol,所以反应的热化学方程式是N2(g)+3H2(g) 2NH3(g)
2NH3(g) 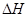 =-92.0kJ/mol。
=-92.0kJ/mol。
考点:考查pH的判断、盐类水解的应用、溶液中离子浓度比较以及反应热的计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,差值对学生灵活运用基础知识解决实际问题的能量的培养。旨在提高学生分析、归纳、总结问题的能力。有利于调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力和抽象思维能力。
本题难度:困难
5、选择题 常温下,用 0.1000 mol・L NaOH溶液滴定 20.00mL0.1000 mol・L
NaOH溶液滴定 20.00mL0.1000 mol・L CH3COOH溶液所得滴定曲线如图。下列说法正确的是
CH3COOH溶液所得滴定曲线如图。下列说法正确的是
A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+ c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:
c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
参考答案:D
本题解析:A、点①反应后溶液是CH3COONa与CH3COOH物质的量之比为1:1的混合物,CH3COOH电离程度大于CH3COO-的水解程度,故c(Na+)>c(CH3COOH),由电荷守恒可知: c(CH3COO-)+c(OH-)=c(Na+)+c(H+),所以c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),故A错;
B、点②pH=7,即c(H+)=c(OH-),由电荷守恒知:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),故c(Na+)=c(CH3COO-),故B错;
C、点③说明两溶液恰好完全反应生成CH3COONa,由于CH3COO-水解,且程度较小,所以c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C错;
D、当CH3COOH较多,滴入的碱较少时,则生成CH3COONa少量,可能出现c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-),故D正确,答案选D。
考点:考查NaOH与CH3COOH的反应中离子浓度比较以及滴定曲线的识别
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,注重答题的灵活性。该题难度较大,对学生的思维能力提出了较高的要求,涉及盐类的水解和溶液离子浓度的大小比较,注意利用电荷守恒的角度解答。
本题难度:困难