时间:2017-08-10 00:43:11
1、选择题 能用键能大小解释的是( )
A.N2的化学性质比O2稳定得多
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而磷酸难挥发
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列说法正确的是( )
A.含有离子键的化合物必是离子化合物
B.含有共价键的物质就是共价化合物
C.共价化合物可能含有离子键
D.离子化合物中不含有共价键
参考答案:A
本题解析:
本题难度:一般
3、填空题 元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
Ⅰ.第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。
镓(31Ga)的基态电子排布式是_________________________________________;
31Ga的第一电离能却明显低于30Zn,原因是______________________________________;
Ⅱ.第四周期过渡元素的明显特征是形成多种多样的配合物。
(1)CO和NH3可以和很多过渡金属形成配合物。CO与N2互为等电子体,CO分子中C原子上有一孤电子对,C、O原子都符合8电子稳定结构,则CO的结构式可表示为________________。NH3 分子中N原子的杂化方式为_______杂化,NH3分子的空间立体构型是____________。
(2)向盛有硫酸铜水溶液的试管中加氨水,首先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加乙醇,析出深蓝色晶体。蓝色沉淀先溶解,后析出的原因是:__________________________________________(用相关的离子方程式和简单的文字说明加以解释)
(3)如图甲所示为二维平面晶体示意图,所表示的化学式为AX3的是________。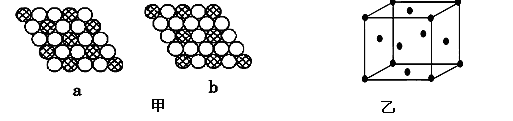
(4)图乙为一个金属铜的晶胞,此晶胞立方体的边长为acm,Cu的相对原子质量为64,金属铜的密度
为ρ g/cm3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。
参考答案:Ⅰ、31Ga的电子排布式是:1s22s22p63s23d104s24p1? (2分)?
30Zn的4s能级处于全充满状态,较稳定?(2分)
Ⅱ、(1)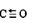 (只写三键没标明配位键的只给1分)(2分) SP3 (1分)?三角锥型(1分)
(只写三键没标明配位键的只给1分)(2分) SP3 (1分)?三角锥型(1分)
(2)蓝色沉淀与氨水可发生如下反应:Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++4H2O+2OH-,
生成的[Cu(NH3)4]SO4在极性较小的乙醇中溶解度较小而析出。(3分)
(方程式正确给2分,其它回答正确也可得3分)
(3)b(2分)
(4)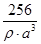 mol-1 ?(2分)
mol-1 ?(2分)
本题解析:Ⅰ、 31Ga的电子排布式是:1s22s22p63s23d104s24p130Zn的4s能级处于全充满状态,较
稳定Ⅱ(1)CO分子中碳和氧共用两对电子,氧提供一对电子配位;NH3是以氮原子为中心,三个氢
原子和氮的一对孤对电子,以sp3不等性杂化方式形成三角锥型
(2) 蓝色沉淀与氨水可发生如下反应:Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++4H2O+2OH-,生成的[Cu(NH3)4]SO4在极性较小的乙醇中溶解度较小而析出。
(3)a图中一个黑的周围有6个相邻白点,一个白的周围有3个相邻黑点,黑:白=1:2
b图中一个黑的周围有6个相邻白点,一个白的周围有2个相邻黑点,黑:白=1:3故选b
(4)金属铜的晶胞为面心立方晶胞,含有6个面心,8个顶点,每个面心是两个晶胞所共用,顶点是8个晶胞所共用,平均每个晶胞中铜原子的个数为6×(1/2)+8×(1/8)=4,每个晶胞4个Cu原子。1mol 的Cu原子质量为64g,1mol的晶胞Cu原子质量就是4X64g
晶胞体积×晶胞密度×阿佛加德罗常数="4×64g" 计算可知:阿佛加德罗常数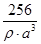 mol-1
mol-1
本题难度:一般
4、填空题 A、B、C、D、E、F是原子序数依次递增的前四周期元素。其中A与D同主族、C与E同主族,且E的原子序数是C的两倍;A分别与B和C均可形成10电子分子;B与C的最外层电子数之比2∶3;F原子的最外层电子数与A相同,其余各层均充满;常见化合物D2C2与水反应生成C的单质,其溶液可使酚酞试液变红。据此回答下列问题:
(1)F元素形成的高价基态离子的核外电子排布式为?;C、D、E三元素原子均能形成简单离子,其离子半径大小顺序为?(用离子符号表示);
(2)A与C形成的10电子分子中含的化学键类型为?(填σ键或π键),分子中心原子的轨道杂化类型为?,其化合物晶体类型为?;化合物A2C和A2E中,沸点较高的是?(填分子式);
(3)向含1 mol A2E的水溶液中加入等物质的量的D2C2,有黄色沉淀生成,写出离子方程式?:
(4)常温常压下,有23 g液态化合物B2A6C与足量的C的单质充分反应,生成BC2气体和A2C液体,同时放出683.5 kJ的热量,该反应的热化学方程式为:?。
参考答案:
(1)? 1s22s22p63s23p63d9或[Ar]3d9? S2-> O2-> Na+ ?(各2分)
(2)σ键? sp3?分子晶体? H2O (各1分)
(3)? Na2O2 +H2S==2Na+ +2OH-?+S↓(3分)
(4)C2H6O(1) + 3O2(g) = 2CO2(g) + 3H2O(1)? ΔH =-1367.0 kJ・mol-1(3分)
本题解析:依题意可知:A为H,B为C,C为O,D为Na,E为S,F为Cu。O2-> Na+,氧离子与钠离子具有相同的核外电子排布,因为钠离子中的质子数比氧离子中的质子数多,所以吸引力强,半径就小。S2-> O2-氧和硫位于同一主族,从上到下,原子半径依次增大,那么相同电荷的阴离子的半径也是从上到下依次增大。向含1 mol A2E的水溶液中加入等物质的量的D2C2,有黄色沉淀生成,此黄色沉淀一定是硫单质。
本题难度:一般
5、选择题 下列有关化学用语正确的是( )
A.丙烯的结构简式:CH2CHCH3
B.乙醇的结构简式:C2H6O
C.四氯化碳的电子式: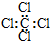
D.乙酸的分子式:C2H4O2
参考答案:A.丙烯的结构简式为CH2=CHCH3,故A错误;
B.乙醇的结构简式为C2H5OH,故B错误;
C.四氯化碳的电子式为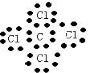 ,故C错误;
,故C错误;
D.乙酸的分子式为C2H4O2,故D正确;
故选D.
本题解析:
本题难度:一般
|