时间:2017-08-10 00:32:10
1、填空题 (10分)下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属, K是一种红棕色气体。

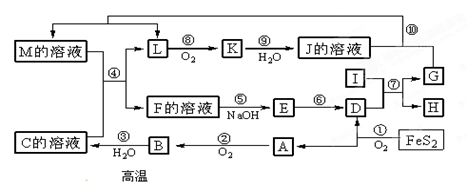
请填写下列空白:
⑴ 在周期表中,组成单质G的元素位于第____________周期_________族。
⑵ 在反应⑦中氧化剂与还原剂的物质的量之比为___________________。
⑶ 在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是___________(填序号)
⑷ 反应④的离子方程式是:__________________________________。
⑸ 将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:_________________________。
参考答案:(1)四(或4);Ⅷ(2分)?(2)1:2(2分)?(3)③(2分)?
(4)3Fe2++NO3-+4H+ = 3Fe3++NO↑+2H2O(2分)?
(5)Fe2O3+3KNO3+4KOH =2K2FeO4+3KNO2+2H2O(2分)
本题解析:I是由第三周期元素组成的单质中熔点最高的金属,则I一定是铝。K是一种红棕色气体,所以K是NO2。因此L是NO。NO2溶于水又生成硝酸和NO,所以J是硝酸。FeS2燃烧生成氧化铁和SO2,所以A是SO2,则D是氧化铁,氧化铁和铝发生铝热反应生成氧化铝互溶单质铁。根据反应⑩可知,反应是氧化还原反应,所以G是铁,H是氧化铝。SO2氧化生成三氧化硫,则B是三氧化硫,三氧化硫溶于水生成硫酸,因此C是硫酸。根据反应④可知,该反应是氧化还原反应,所以M应该是硝酸亚铁,则F是铁盐,所以E是氢氧化铁,氢氧化铁分解生成氧化铁。
点评:化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。
本题难度:一般
2、选择题 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去)。则W、X不可能是?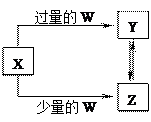
| 选项 | W | X |
| A | 盐酸 | Na2CO3溶液 |
| B | Cl2 | Fe |
| C | CO2 | Ca(OH)2溶液 |
| D | NaOH | AlCl3溶液 参考答案: 本题解析: 本题难度:一般 3、填空题 (12分)某短周期元素的原子最外层电子数为次外层的2倍,其单质甲可发生如下反应:甲+乙 参考答案: 本题解析:略 本题难度:困难 4、填空题 在下列各变化中,E为常温下无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略). 参考答案:E为常温下无色无味的液体且在生成物中,所以是水.F为淡黄色粉末,是过氧化钠或硫,但能和水反应,所以是过氧化钠.过氧化钠和水反应的生成物是氧气和氢氧化钠,G为常见的无色气体,所以G是氧气,H是氢氧化钠. 本题解析: 本题难度:一般 5、推断题 下图是物质A-K的相互转变关系图。已知A是由原子个数比为1:2:4的三种常见元素组成的化合物,在隔绝空气下A加热分解得到等物质的量的B、C、D三种氧化物;常温下B、C、F是无色气体,J为黄绿色气体,G、H为常见金属单质,部分反应条件未注明。 参考答案:(l)FeC2O4 本题解析: 本题难度:一般 |