时间:2017-08-10 00:24:51
1、选择题 下列图像正确的是?(?)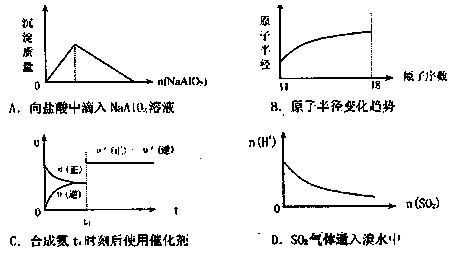
参考答案:C
本题解析:略
本题难度:一般
2、选择题 下列说法不合理的是
A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗
B.在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性
C.用纸上层析法检验氯化铁溶液中是否混有少量氯化铜
D.硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分摩擦器皿壁促使晶体析出
参考答案:B
本题解析:A.容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无"0"刻度,滴定管有"0"刻度;关于仪器标识的叙述是正确的。使用时滴定管水洗后还需润洗,否则所盛溶液的浓度要改变,但容量瓶水洗后不用润洗,否则所配溶液浓度变大;A合理;B.在两支试管中分别加1mL无水乙醇和1.5g苯酚固体,再加等量等体积的钠,比较乙醇、苯酚羟基上氢原子的活泼性,由于初始条件不同,无法得出正确的结论,B不正确;C.纸上层析法适用于微量分离和检验化学性质十分相近的分子或离子,用纸上层析法检验氯化铁溶液中是否混有少量氯化铜,C合理;D.加入晶体、摩擦烧杯壁,产生玻璃碎末、过度冷却、用玻璃棒搅拌这样都可以找一个“中心”聚集起来让晶体析出,硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分摩擦器皿壁促使晶体析出,D正确;选B。
本题难度:一般
3、实验题 某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L H2SO4溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,则至少需要称量NaOH固体?g。
(2)从下图中选择称量NaOH固体所需要的仪器(填序号)?。
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 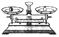 |  |  |  |  | 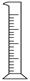 |
| 序号 | a | b | c | d | e | f |
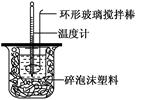
| 温度 实验次数 | 超始温度t1/℃ | 终止温度t2/℃ | 平均温度差 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ? |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
参考答案:Ⅰ(1)5.0?(2)abe?
Ⅱ(1)1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l)? ΔH="-57.3KJ/mol" (2) ①? 4.0?②a c d
本题解析:Ⅰ(1)容量瓶与245 mL NaOH溶液接近的规格是250 mL的。溶液有均一性,各处的浓度相同。n(NaOH)="V・C=0.25L×0.50" mol/L="0.125" mol.m(NaOH)="n・M=0.125" mol×40g/mol=5.0g.(2)称量固体药品要用天平、药匙。由于氢氧化钠有腐蚀性所以不能直接用天平来称量,要放在烧杯中称量。因此称量NaOH固体所需要的仪器代码是a b eⅡ(1)中和热是酸碱发生反应产生1摩尔的水时放出的热。强酸与强碱发生中和反应表示中和热的热化学方程式为:1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l)? ΔH="-57.3KJ/mol" (2)①分析上述四组数据可以看出:第二组数据误差太大,要去掉。求出其余三组数据的温度差的平均值就是平均温度差。{(30.1-26.1)+(29.8-25.9)+(30.4-26.3)}÷3=4.0。②中和热的实验值为53.5 kJ/mol比中和热的理论值57.3 kJ/mol小,可能的原因是a.实验装置保温、隔热效果差。c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度。对于b.在量取NaOH溶液的体积时仰视读数,则氢氧化钠的体积偏小,产生的水的物质的量偏小中和热的数值就偏大。与题干相违背。故测定的中和热偏小的原因是a c d。
本题难度:一般
4、实验题 (16分)
Ⅰ.下列操作正确的是_______.
A.用氨水清洗做过银镜反应的试管
B.用酒精清洗有硫沉淀的试管
C.用碱式滴定管量取20.00 mL 0.1000 mol/L KMnO4溶液;
D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
E、如果苯酚浓溶液沾到皮肤上,应立即用70℃以上的水清洗
F、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
G、用托盘天平称取10.50 g干燥的NaCl固体;
H、向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
I、配制Al2(SO4)3溶液时,加入少量的稀硫酸。
Ⅱ.用下图装置进行SO2转化为SO3的转化率测定实验:?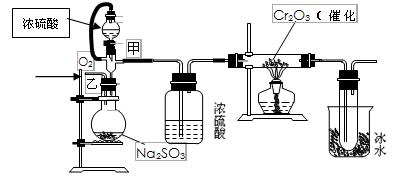
(1)写出圆底烧瓶中发生反应的化学方程式?
(2)实验前,必须进行的操作是(填操作名称,不必写具体过程) ? 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时滴入浓硫酸与加热催化剂的先后顺序是?。
(4)本实验装置设计中有不恰当的地方,请指出: ? ? 。
所增加装置的目的是 ? ? 。
(5)将反应生成的44.8L(标况下)SO2气体全部通过硬质玻璃管后,在右侧烧杯的试管中得到152g固体,则SO2的转化率为?
参考答案:(16分)
Ⅰ.F、I(4分)
Ⅱ.(1)Na2SO3+H2SO4(浓)==NaSSO4+SO2↑+H2O?(2分)
(2)查装置的气密性?(2分)
(3)先加热催化剂,然后缓慢滴加浓硫酸?(2分)
(4)需要增加尾气吸收装置,(2分)吸收未反应的SO2,防止污染环境(2分)
(5)95% (2分)
本题解析:略
本题难度:一般
5、选择题 某课外实验小组的同学们采取的下列实验操作中,正确的是
①甲同学用手取氯化钠;②乙同学用灯帽盖灭酒精灯;③丙同学给30 mL试管中的20 mL液体加热;④丁同学用酒精萃取碘水中的碘;⑤戊同学将浓硫酸倒入装有适量水的量筒中稀释;⑥己同学配制NaOH溶液时,将NaOH固体在烧杯中溶解后,立即注入容量瓶中。
A.只有②
B.只有①②③
C.只有⑤⑥
D.全部正确
参考答案:A
本题解析:①错,不能用手直接接触药品;②正确;③错,有试管加热液体,其体积不能超过试管容积的1/3;④错,酒精不能作为萃取剂;⑤错,量筒不能用于配制溶液;⑥错,应溶解冷却室温后再倒入容量瓶;
本题难度:一般
1、选择题 玻璃棒是化学实验中的常用仪器,下列实验需要用到玻璃棒的正确组合是①测溶液pH②配制500mL 0.1mol/L NaC1溶液③中和和滴定④焰色反应⑤过滤⑥蒸馏?(?)
A.①②④⑤
B.②③④
C.①②⑤
D.①②⑤⑥
2、选择题 下列实验操作中,错误的是(1)用托盘天平称取5.2gNaCl ;(2)用50mL量筒量取5.2mL盐酸;(3)用蒸发皿加热KNO3溶液制取KNO3晶体;(4)用100mL容量瓶配制50mL0.1mol/LH2SO4溶液;(5)用带玻璃塞的棕色试剂瓶存放浓HNO3;(6)用煤油液封保存锂、钠、钾单质
A.(2)(3)(5)
B.(2)(4)(5)
C.(1)(4)(6)
D.(2)(4)(6)
3、选择题 下列实验所用的试纸不能预先用蒸馏水润湿的是
A.用品红试纸检验SO2
B.用淀粉碘化钾试纸检验C12
C.用红色石蕊试纸检验NH3
D.用pH试纸测定某溶液的pH
4、选择题 下列有关实验操作的叙述正确的是(? )?
A.用50 mL酸式滴定管可准确量取25.00 mLKMnO4溶液
B.用量筒量取5.00 mL 1.00 mol・L-1盐酸于50 mL 容量瓶中,加水稀释至刻度,可配制0.100 mol・L-1盐酸
C.用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出
D.实验室常用向沸水中逐滴加入饱和FeCl3溶液,持续加热的方法制备氢氧化铁胶体
5、选择题 利用下列装置(部分仪器已省略),能顺利完成对应实验的是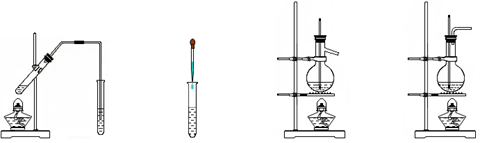
A.制硝基苯
B.制氢氧化亚铁
C.实验室制乙烯
D.石油的蒸馏