ʱ��:2017-08-10 00:21:34
1��ѡ���� 2007��ŵ������ѧ������ߵ¹���ѧ�Ҹ���¡����ض��ڱ��滯ѧ�о����������˿����Թ��ס���ѧ�ҽ��о���������壨��Һ�壩�ڽ�������������������ѧ����Ŀ�ѧ��Ϊ���滯ѧ��������������о������ڱ��滯ѧ�������
A���Ȼ�����ˮ�е��ܽ�ƽ��
B������ȼ�ϵ���е缫�ϵķ�Ӧ
C�����ڳ�ʪ�Ŀ���������
D������������������ý�����»���
�ο��𰸣�A
��������������ǿ�������滯ѧ����������룬ֻ��Aѡ����ܽ�ƽ���������أ��ʲ������滯ѧ���롣
�����Ѷȣ�һ��
2������� ��12�֣��й�����ļ������⡣
��1��H2S�ڿ����п���ȼ�ա�
��֪���� 2H2S(g) + O2(g)  2S(s) + 2H2O(g) ��H= ��442.38 kJ/mol
2S(s) + 2H2O(g) ��H= ��442.38 kJ/mol
��S(s) + O2(g)  SO2(g) ��H= ��297.04 kJ/mol
SO2(g) ��H= ��297.04 kJ/mol
H2S(g)��O2(g)��Ӧ����SO2(g)��H2O(g)���Ȼ�ѧ����ʽ�� ��
��2��SO2�Ǵ�����Ⱦ���ˮ�������õ�����SO2����������������¡�
�� SO2���ں�ˮ����H2SO3��H2SO3���ջ�����SO32��������뷽��ʽ�� ��
�� SO32�����Ա���ˮ�е��ܽ�������ΪSO42������ˮ��pH�� ������ߡ� �������䡱���͡�����
�� Ϊ������ˮ��pH���ɼ������ʵĺ�ˮ��ʹ���е�HCO3�����뷴Ӧ���䷴Ӧ�����ӷ���ʽ�� ��
�� ��������Ӧ��ͬʱ��Ҫ���������������ԭ���� ��
��3����Ȼ��ر���ԭ��ͭ�����ᆳ�������������ú���CuSO4��Һ���������������������ܵ�ZnS������ת��Ϊͭ����CuS�����û�ѧ�����ʾ��ZnSת��ΪCuS�Ĺ��̣� ��
�ο��𰸣���1��2H2S(g)+3O2(g)  2SO2(g)+2H2O(g) ��H= ��1036.46 kJ/mol ��2���� H2SO3
2SO2(g)+2H2O(g) ��H= ��1036.46 kJ/mol ��2���� H2SO3 HSO3��+ H+ HSO3��
HSO3��+ H+ HSO3�� SO3 2��+ H+ ��ÿ��1�֣���2�֣� �� ���� �� HCO3 ��+ H+
SO3 2��+ H+ ��ÿ��1�֣���2�֣� �� ���� �� HCO3 ��+ H+  CO2 ��+ H2O��2�֣�
CO2 ��+ H2O��2�֣�
���������ˮ���ܽ�������SO32-������ΪSO42-��������ƽ��H2SO3 HSO3��+ H+ HSO3��
HSO3��+ H+ HSO3�� SO3 2��+ H+ �����ƶ�����߶��������ת���ʣ�ͬʱ�ӿ췴Ӧ���ʵ����á���3��CuSO4
SO3 2��+ H+ �����ƶ�����߶��������ת���ʣ�ͬʱ�ӿ췴Ӧ���ʵ����á���3��CuSO4 Cu 2++SO42-��ZnS��s��
Cu 2++SO42-��ZnS��s�� Zn(aq) +S2-(aq)��Cu 2(aq)++ S2-(aq)
Zn(aq) +S2-(aq)��Cu 2(aq)++ S2-(aq)  CuS��s��
CuS��s��
�����������1������+�ڡ�2�ɵ�H2S(g)��O2(g)��Ӧ�Ļ�ѧ����ʽ�����䦤H=��442.38 kJ/mol+ ����297.04 kJ/mol ����2=��1036.46 kJ/mol������H2S(g)��O2(g)��Ӧ����SO2(g)��H2O(g)���Ȼ�ѧ����ʽ�ǣ�2H2S(g)+3O2(g)  2SO2(g)+2H2O(g) ��H= ��1036.46 kJ/mol ����2����H2SO3�Ƕ�Ԫ��ǿ�ᣬ�ֲ����롣���뷽��ʽΪ��H2SO3
2SO2(g)+2H2O(g) ��H= ��1036.46 kJ/mol ����2����H2SO3�Ƕ�Ԫ��ǿ�ᣬ�ֲ����롣���뷽��ʽΪ��H2SO3 HSO3��+ H+ ��HSO3��
HSO3��+ H+ ��HSO3�� SO3 2��+ H+ �ڻᷢ����Ӧ��2SO2+ 2H2O+O2
SO3 2��+ H+ �ڻᷢ����Ӧ��2SO2+ 2H2O+O2 2H2SO4��������ǿ������pH���͡����ܽ���SO2�ĺ�ˮ�����ԣ���HCO3 ����Ӧ�����ӷ���ʽΪHCO3 ��+ H+
2H2SO4��������ǿ������pH���͡����ܽ���SO2�ĺ�ˮ�����ԣ���HCO3 ����Ӧ�����ӷ���ʽΪHCO3 ��+ H+  CO2 ��+ H2O ���ܴ�����������������������Ũ�ȣ���SO32-������ΪSO42-��������ƽ��H2SO3
CO2 ��+ H2O ���ܴ�����������������������Ũ�ȣ���SO32-������ΪSO42-��������ƽ��H2SO3 HSO3��+ H+ HSO3��
HSO3��+ H+ HSO3�� SO3 2��+ H+ �����ƶ�����߶��������ת���ʣ�ͬʱ�ӿ췴Ӧ���ʵ����á���3��CuSO4����ZnSת��ΪCuS��һ��������ת�����̣��ܽ�ȴ�ij���ת��Ϊ�ܽ��С�ij����������ķ�Ӧ�У�CuSO4
SO3 2��+ H+ �����ƶ�����߶��������ת���ʣ�ͬʱ�ӿ췴Ӧ���ʵ����á���3��CuSO4����ZnSת��ΪCuS��һ��������ת�����̣��ܽ�ȴ�ij���ת��Ϊ�ܽ��С�ij����������ķ�Ӧ�У�CuSO4 Cu 2++SO42-��ZnS��s��
Cu 2++SO42-��ZnS��s�� Zn(aq) +S2-(aq)��Cu 2+(aq)+ S2- (aq)
Zn(aq) +S2-(aq)��Cu 2+(aq)+ S2- (aq) CuS��s��
CuS��s��
���㣺�Ȼ�ѧ����ʽ�ļ��㡢���ӷ���ʽ����д�ͳ���ת����
�����Ѷȣ�����
3������� ��ѧ�����õ�ˮ�뺣ˮ֮�京�����IJ������һ�����͵�ء���ˮ��ء�
��1���ö����������װ��������������߷���Ч�ʣ������������ײ��ϵ�����?�������ԣ�ʹ֮���������ӳ�ֽӴ���
��2��ˮ����ܷ�Ӧ�ɱ�ʾΪ��5MnO2��2Ag��2NaCl��Na2Mn5O10��2AgCl���õ�صĸ�����ӦʽΪ��������������������������ˮ��ع���ʱ��Na��������?�������ƶ���
��3��ˮ�������1 mol Na2Mn5O10ת�Ƶ��ӵ����ʵ���Ϊ?��
��4��ij�¶��£�Fe��OH��3��s����Mg��OH��2��s���ֱ�����Һ�дﵽ�����ܽ�ƽ�����Һ�н��������ӵ�Ũ������ҺpH�Ĺ�ϵ����ͼ�������ͼ������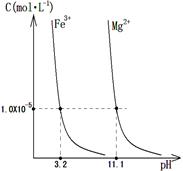
�ٸ��¶��£��ܶȻ������Ĺ�ϵΪ��KSP[Fe��OH��3]?KSP[Mg��OH��2]�����������������������
������������ɵ�Mg��OH��2��Һ�е���������FeCl3��Һ����ɫ������ȫ��ת��Ϊ���ɫ������ԭ����?��
�ο��𰸣���1����ǿ������������ϴ�ı����?��2�֣�
��2��Ag + Cl����e����AgCl ��3�֣�2�����������ӡ��������۷֣�����дAg+�����֣� ����2�֣�
��3��2 mol��3�֣���λ��©��1�֣�?��4���� �� ��2�֣�
��Mg��OH��2��Һ�д��ڳ����ܽ�ƽ�⣨1�֣���Mg��OH��2��s��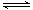 Mg2+��aq��+2OH����aq��������������FeCl3��Һ��c��Fe3+����c3��OH�D����KSP[Fe��OH��3],Fe3+��OH�����ɸ����ܵ�Fe��OH��3��1�֣���ʹMg��OH��2��Һ�����ܽ�ƽ�������ƶ���1�֣���Mg��OH��2��Һת��ΪFe��OH��3������1�֣�����ע��Ҫ�㣬���������֣�
Mg2+��aq��+2OH����aq��������������FeCl3��Һ��c��Fe3+����c3��OH�D����KSP[Fe��OH��3],Fe3+��OH�����ɸ����ܵ�Fe��OH��3��1�֣���ʹMg��OH��2��Һ�����ܽ�ƽ�������ƶ���1�֣���Mg��OH��2��Һת��ΪFe��OH��3������1�֣�����ע��Ҫ�㣬���������֣�
�����������1���������ײ��ϵı�������к�ǿ����������������ʹ֮���������ӳ�ֽӴ�����߷���Ч�ʡ�
��2��ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ�������ܷ�Ӧʽ5MnO2��2Ag��2NaCl��Na2Mn5O10��2AgCl��֪��MnԪ�صĻ��ϼ۴ӣ�4�۽��͵���3.6�ۣ��õ���������������AgԪ�صĻ��ϼ۴�0�����ߵ���1��ʧȥ��������ԭ�����������Ǹ������缫��ӦʽΪAg + Cl����e����AgCl��ˮ��ع���ʱ��������Na�����������������ƶ���
��3��MnԪ�صĻ��ϼ۴ӣ�4�۽��͵���3.6�ۣ�����ˮ�������1 mol Na2Mn5O10ת�Ƶ��ӵ����ʵ���Ϊ1mol��5����4��3.6����2mol��
��4���ٸ���ͼ���֪���ڽ��������ӵ����ʵ���Ũ����ͬ������£�����������Ӧ��pHС��������þ��Ӧ��pHֵ�����������������ܶȻ�����С��������þ���ܶȻ�������
������Mg��OH��2��Һ�д��ڳ����ܽ�ƽ��Mg��OH��2��s��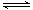 Mg2+��aq��+2OH����aq��������������FeCl3��Һ������Һ��c��Fe3+����c3��OH�D����KSP[Fe��OH��3]ʱ,Fe3+��OH�����ɸ����ܵ�Fe��OH��3��ʹMg��OH��2��Һ�ij����ܽ�ƽ�������ƶ����Ӷ�ʹMg��OH��2��Һȫ��ת��ΪFe��OH��3������
Mg2+��aq��+2OH����aq��������������FeCl3��Һ������Һ��c��Fe3+����c3��OH�D����KSP[Fe��OH��3]ʱ,Fe3+��OH�����ɸ����ܵ�Fe��OH��3��ʹMg��OH��2��Һ�ij����ܽ�ƽ�������ƶ����Ӷ�ʹMg��OH��2��Һȫ��ת��ΪFe��OH��3������
�����Ѷȣ�һ��
4������� ij����ˮ�к���Ca2+��Mg2+��Na+��K+����HCO32����SO42����Cl��������������������ˮ���ڹ�¯���γ�ˮ������¯ˮ�������ķ�ȼ�ϣ��������ջ���¯��Σ�գ����Ҫ���������¯ˮ������֪��������20��ʱ���ܽ������Ϊ��
(1)���û�ѧ����ʽ��ʾ��¯�е�ˮ������Mg(OH)2��ԭ��_________________________?��
(2)��¯�е�ˮ�������е�CaSO4����ֱ�������ȥ����Ҫ�����Լ�X��ʹ��ת��Ϊ���������������Y����ȥ���Լ�X��_____________ (�����)��
A��ʳ��
B���Ȼ���
C��̼����
D��̼������
(3)ˮ�е�Ca2+��Mg2+������һ��Ũ�ȵ�M��Һ���вⶨ��M��Ca2+��Mg2+���Ե����ʵ������з�Ӧ����ȡ��Ca2+Ũ��Ϊ0.40g/L������ˮ��10mL������ƿ�н��еζ����ﵽ�յ�ʱ����ȥ��Ũ��Ϊ0.01mol/L��M��Һ20.00 mL���������ˮ����Mg2+�����ʵ���Ũ����______________________________��
�ο��𰸣�(1)Mg(HCO3)2 MgCO3��+H2O+CO2����? MgCO3+H2O
MgCO3��+H2O+CO2����? MgCO3+H2O Mg(OH)2+CO2��
Mg(OH)2+CO2��
(2)C?(3)0.01mol/L
�����������1����Ϊ�ڼ��ȵ�������̼����þ��ֽ�����̼��þ���������ȣ�̼��þ���Ժ�ˮ����ˮ�ⷴӦ����������þ��
��2���Ƶ�̼�������������ᣬ���Կɼ���̼���ƣ�����̼��ƶ���ȥ��
��3��10ml����ˮ�к��и����ӵ����ʵ����� ��
��
ͬʱ����MҲ��0.0001mol��M�ܵ����ʵ�����0.01mol.L��0.02L��0.0002mol�����Ժ�þ���ӷ�Ӧ��M��0.0002mol��0.0001mol��0.0001mol����þ������0.0001mol��������Ũ��Ϊ
�����Ѷȣ�һ��
5������� �ڽ���θ����ʱ��Ϊȡ�����õļ��Ч������Ҫ�ڼ��֮ǰ���á����͡��������͡�����Ҫ�ɷ������ᱵ����25��ʱ��1Lˮ��Լ���ܽ�2.4��10-3g?���ᱵ�������ܶȻ�����Ksp=1.1��10-10��
��1����������һ���ж����ؽ������ӣ��������б�����Ũ�ȴﵽ2��10-3mol?L-1ʱ���ͻ�Խ�������Σ������ͨ������˵��Ϊʲô���������ᱵ��Ϊ�����͡���
��2����25��ʱ��1Lˮ��Լ���ܽ�0.018g?̼�ᱵ����θҺ�����Եģ��ܷ���̼�ᱵ�������ᱵ��Ϊ�����͡�����Ҫ�ɷ֣�
�ο��𰸣���1���������ᱵ���ܽ�ƽ����㣬�����ᱵ�д���ƽ�⣺BaSO4��s��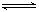
?Ba2+��aq��+SO42-��aq����
c��Ba2+��=
���������
�����Ѷȣ�һ��