时间:2017-08-09 23:58:10
1、选择题 下列溶液中,微粒浓度关系正确的是( )
A.含有NH4+、Cl-、H+、OH-离子的溶液中,其离子浓度一定是:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.pH=8的氨水与氯化铵的混合溶液中:c(Cl-)>c(NH4+)
C.0.1mol/L的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S)
D.pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)=c(H+)
参考答案:A.含有NH4+、Cl-、H+、OH-离子的溶液中,可能为一水合氨和氯化铵的混合溶液,则可能存在c(NH4+)>c(Cl-)>c(OH-)>c(H+),故A错误;
B.pH=8的氨水与氯化铵的混合溶液,显碱性,由电荷守恒c(NH4+)+c(H+)=c(Cl-)+c(OH-)可知,c(Cl-)<c(NH4+),故B错误;
C.由质子守恒可知,c(OH-)=c(H+)+c(HS-)+2c(H2S),故C正确;
D.一元酸,为强酸或弱酸,则pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)≤c(H+),故D错误;
故选C.
本题解析:
本题难度:一般
2、选择题 下列溶液中微粒的物质的量浓度关系正确的是( )
A.NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-)
B.pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后的溶液中:c(H+)>c(OH-)
C.0.1mol/L的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中:2c(Na+)=c(CH3COOH)+c(CH3COO-)
参考答案:BD
本题解析:
本题难度:一般
3、选择题 常温下,向20mL某盐酸溶液中逐滴加入0.1mol/L的氨水,溶液pH的变化与加入氨水的体积关系如图所示,下列叙述正确的是( )
A.盐酸的物质的量浓度为1mol/L
B.在①、②之间的任意一点:c(Cl-)>c(NH4+),c(H+)>c(OH-)
C.在点②所示溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+),且V<20
D.在点③所示溶液中:由水电离出的c(OH-)>10-7mol/L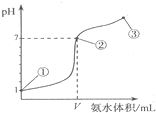
参考答案:B
本题解析:
本题难度:一般
4、选择题 物质的量浓度相同的下列溶液,pH由大到小排列正确的是
[? ]
A.Ba(OH)2、Na2SO3、FeCl3、KCl
B.Na2SiO3、Na2CO3、KNO3、NH4Cl
C.NH3·H2O、H3PO4、Na2SO4、H2SO4
D.NaHCO3、C6H5COOH、C2H5OH、HCl
参考答案:B
本题解析:
本题难度:一般
5、选择题 下列各溶液中,物质的量浓度关系正确的是( )
A.在0.1?mol?L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
B.常温下,10?mL?0.01?mol?L-1HCl溶液与10?mL?0.01?mol?L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20?mL,则溶液的pH=12
C.0.1?mol?L-1的KAl(SO4)2溶液中:c(SO42-)>c(Al3+)>c(OH-)>c(H+)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液,若溶液呈酸性,则有c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
参考答案:A、在0.1?mol?L-1CH3COONa溶液中,存在质子守恒:c(OH-)=c(CH3COOH)+c(H+),故A正确;
B、常温下,10?mL?0.01?mol?L-1HCl溶液与10?mL?0.01?mol?L-1Ba(OH)2溶液充分混合后,碱剩余,剩余氢氧根的浓度=0.01mol/L×2×0.01L-0.01mol/L×0.01L0.02L=0.005mol/L,
所以氢离子浓度c=Kwc(OH-)=1×10-140.005=2×10-12mol/L,所以pH=12-lg2=11.7,故B错误;
C、0.1?mol?L-1的KAl(SO4)2溶液中,铝离子水解导致溶液显示酸性,所以c(OH-)<c(H+),即c(SO42-)>c(Al3+)>c(H+)>c(OH-),故C错误;
D、等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液,根据溶液呈酸性,则证明HX的电离程度大于NaX中X-的水解程度,所以c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-),故D错误.
故选A.
本题解析:
本题难度:一般