时间:2013-06-15 15:33:44
34、(8分)【生物――生物技术实践】
胡萝卜素是一种常见的食物色素,可分别从胡萝卜或产生胡萝卜素的微生物菌体中提取获得,流程如下:
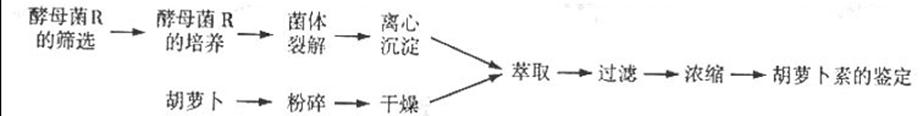
(1)筛选产胡萝卜素的酵母菌R时,可选用 或平板划线法接种。采用平板划线法接种时需先灼烧接种环,其目的是 。
(2)培养酵母菌R时,培养基中的蔗糖和硝酸盐可分别为酵母菌R的生长提供 和 。
(3)从胡萝卜中提取胡萝卜素时,干燥过程应控制好温度和 以防止胡萝卜素分解;萃取过程中宜采用 方式加热以防止温度过高;萃取液浓缩前需进行过滤,其目的是 。
(4)纸层析法可用于鉴定所提取的胡萝卜素。鉴定过程中需用胡萝卜素标准品作为 。
35、(8分)【生物――现代生物科技专题】
科学家通过诱导黑鼠体细胞去分化获得诱导性多能干细胞(iPS),继而利用iPS细胞培育出与黑鼠遗传特性相同的克隆鼠,流程如下:
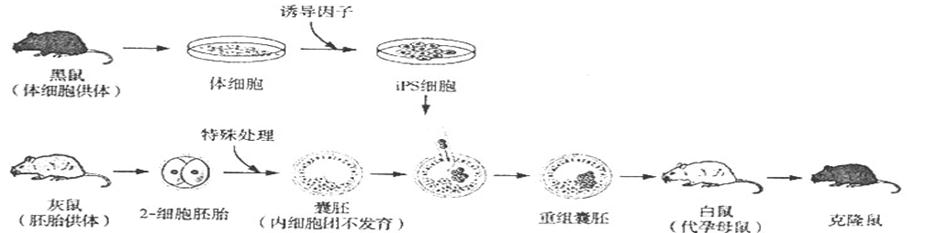
(1)从黑鼠体内获得体细胞后,对其进行的初次培养称为 ,培养的细胞在贴壁成长至充链满培养皿底时停止分裂,这种现象称为
(2)图中2―细胞胚胎可用人工方法从灰鼠输卵管内获得,该过程称为 ,也可从灰鼠体内取出卵子,通过 后进行早期胚胎培养获得。
(3)图中重组囊胚通过 技术移入白鼠子宫内继续发育,暂不移入的胚胎可使用 方法保存。
(4)小鼠胚胎干细胞(ES)可由囊胚的 分离培养获得,iPS与ES细胞同样具有发育全能性,有望在对人类iPS细胞进行定向 后用于疾病的细胞治疗。
36.(8分)(物理选修3-3)
(1)下列关于热现象的描述正确的是( )
a.根据热力学定律,热机的效率可以达到100%
b.做功和热传递都是通过能量转化的方式改变系统内能的
c.温度是描述热运动的物理量,一个系统与另一个系统达到热平衡时两系统温度相同
 d.物体由大量分子组成,其单个分子的运动是无规则的,大量分子的运动也是无规律的
d.物体由大量分子组成,其单个分子的运动是无规则的,大量分子的运动也是无规律的
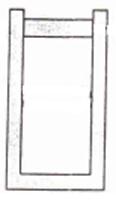
(2)我国“蛟龙”号深海探测船载人下潜超七千米,再创载人深潜新纪录。在某次深潜实验中,“蛟龙”号探测到990m深处的海水温度为280K。某同学利用该数据来研究气体状态随海水温度的变化,如图所示,导热性良好的气缸内封闭一定质量的气体,不计活塞的质量和摩擦,气缸所处海平面的温度To=300K,压强P0=1 atm,封闭气体的体积Vo=3m2。如果将该气缸下潜至990m深处,此过程中封闭气体可视为理想气体。
①求990m深处封闭气体的体积(1 atm相当于10m深的海水产生的压强)。
②下潜过程中封闭气体___________(填“吸热”或“放热”),传递的热量__________(填“大于”或“小于”)外界对气体所做的功。
 37.(8分)(物理选修3-4)
37.(8分)(物理选修3-4)
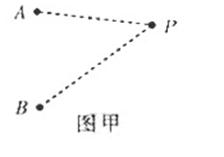
(1)如图甲所示,在某一均匀介质中,A、B是振动情况完全相同的两个波源,其简谐运动表达式为![]() 介质中P点与A、B两波源间距离分别为4M和5M,两波源形成的简谐横波分别沿AP、BP方向传播,波速都是10m/s。
介质中P点与A、B两波源间距离分别为4M和5M,两波源形成的简谐横波分别沿AP、BP方向传播,波速都是10m/s。
①求简谐横波的波长。
②P点的振动__________(填“加强”或“减弱”)
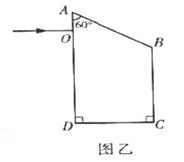 (2)如图乙所示,ABCD是一直角梯形棱镜的横截面,位于截面所在平面内的一束光线由O点垂直AD边射入。已知棱镜的折射率
(2)如图乙所示,ABCD是一直角梯形棱镜的横截面,位于截面所在平面内的一束光线由O点垂直AD边射入。已知棱镜的折射率![]() 。
。
①求光线第一次射出棱镜时,出射光线的方向。
②第一次的出射点距C_____cm。
38、(8分)(物理选修3-5)
(1)恒星向外辐射的能量来自于其内部发生的各种热核反应,当温度达到108 K时,可以发生“氦燃烧”。
①完成“氦燃烧”的核反应方程:![]() 。
。
②![]() 是一种不稳定的粒子,其半衰期为2.6*10-16s。一定质量的
是一种不稳定的粒子,其半衰期为2.6*10-16s。一定质量的![]() ,晶7.8*10-16s后所剩
,晶7.8*10-16s后所剩![]() 占开始时的_______。
占开始时的_______。
(2)如图所示,光滑水平轨道上放置长坂A(上表面粗糙)和滑块C,滑块B至于A的左端,三者质量分别为MA=5kg、MB=1kg、MC=2kg。开始时C静止,A、B一起一![]() 速度匀速向右运动,A与C发生碰撞(事件极短)后C向右运动,经过一段时间A、B再次达到共同速度一起向右运动,且恰好不再与C碰撞。求A与C发生碰撞后瞬间A的速度大小。
速度匀速向右运动,A与C发生碰撞(事件极短)后C向右运动,经过一段时间A、B再次达到共同速度一起向右运动,且恰好不再与C碰撞。求A与C发生碰撞后瞬间A的速度大小。