时间:2017-07-27 08:12:04
1、选择题 下列描述中,不符合生产实际的是( )
A.合成氨工业中,N2和H2的最佳配比应为物质的量之比1:3
B.电解法精炼粗铜,用纯铜作阴极
C.工业上电解饱和食盐水制烧碱,用离子交换膜阻止0H-移向阳极
D.在镀件上电镀锌,锌作阳极
参考答案:A、合成氨工业中,氮气比较廉价,为了提高氢气的转化率要加入过量的氮气,所以N2和H2的物质的量之比大于1:3,故A错误.
B、电镀时,镀层作阳极,镀件作阴极,所以纯铜作阴极,粗铜作阳极,故B正确.
C、工业上电解饱和食盐水制烧碱,溶液中阴离子向阳极移动,阳离子向阴极移动,用离子交换膜阻止0H-移向阳极,故C正确.
D、电镀时,镀层作阳极,镀件作阴极,镀层为锌,所以锌作阳极,故D正确.
故选A.
本题解析:
本题难度:简单
2、选择题 pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是( )
A.Na2SO4
B.H2SO4
C.AgNO3
D.NaOH
参考答案:A、电解硫酸钠溶液时,实际上电解的是水,所以溶液中氢离子和氢氧根离子的相对浓度不变,只是硫酸钠的浓度增大,故pH值不变,故A错误;
B、电解硫酸溶液时,实际上电解的是水,但溶液中氢离子的浓度增大,pH值减小,故B错误;
C、电解硝酸银溶液时,阴极上析出银,阳极上得到氧气,所以溶液中的氢氧根离子的浓度减小,氢离子的浓度增大,溶液的pH值减小,故C错误;
D、电解氢氧化钠溶液时,实际上电解的是水,但溶液中的氢氧根离子的浓度增大,氢离子的浓度减小,所以溶液的Pp值增大,故D正确;
故选D.
本题解析:
本题难度:简单
3、填空题 (7分)如图,将铜片和锌片焊接在一起组成A电极,B为碳棒进行电解实验,电解液中含硝酸银和硝酸铜各0.1 mol。已知电路中通过0.2 mol电子。
(1)请写出A.B两极发生反应的电极反应式A:?B:?
(2)请分析A.B两极质量变化情况为A:___________B:__________?
参考答案:(1)A:Zn-2e-=Zn2+(1分) B:先2Ag++2e-?="2Ag?" 后Cu2++2e-?=Cu(各1分)
(2)(各2分)A极减少6.5克,? B极增加14克。
本题解析:略
本题难度:简单
4、简答题 2011年3月12日,日本因大地震导致福岛核泄漏,主要泄漏物为碘131和绝137.在被辐射地区,每天服用一片碘片可以起到一定的预防作用.因此世界多地出现市民抢购碘片现象,我国部分地区还出现抢购加碘食盐现象.为此卫生部有关专家指出市民不应擅自服用碘片,多吃碘盐也起不到预防放射性碘辐射的作用,且我国碘盐丰富,不必抢购.碘片和碘盐相关信息:
碘片:主要成分是碘化钾,每片含100毫克的碘,防核辐射每天服一片.
碘盐:加碘食盐,主要成分是氯化钠、碘酸钾,每公斤食用盐中碘含量为20-30毫克.
KIO3可用电解法制得:以石墨为阳极,不锈钢为阴极,在一定温度和电流下电解KI溶液,
总反应方程式为:KI+3H2O?
? |
参考答案:(1)碘127和碘131中质子数相同而中子数不同,属于同位素,每片碘片含100毫克的碘,而每公斤食用盐中碘含量为20毫克,所以人每天吃100mg20mg=5公斤盐才相当于服用一片碘片,说明靠吃碘盐来预防放射性碘无作用,
故答案为:中子数;5;无;
(2)电解法制KIO3中,阳极发生氧化反应,电极反应式为I-+3H2O-6e-=IO3-+6H+,阴极反应式为:2H2O+2e-=H2↑+2OH-,阴极PH增大,
故答案为:I-+3H2O-6e-=IO3-+6H+;增大;
(3)①IO3-具有氧化性,在酸性条件下与具有还原性的I-发生氧化还原反应生成I2,反应的离子方程式为IO3-+5I-+6H+=3I2+3H2O,
故答案为:IO3-+5I-+6H+=3I2+3H2O;
②根据反应IO3-+5I-+6H+=3I2+3H2O,以及I2+2S2O32-(无色)→2I-+S4O62-(无色),得出反应的关系式IO3-~3I2~6S2O32-,
又n(Na2S2O3)=0.010mol/L×0.012L=0.00012mol,
则IO3-~3I2~6S2O32-
? 1? 6
n(IO3-)? 0.00012mol
n(IO3-)=0.00002mol,
m(KIO3)=0.00002mol×214g/mol=0.00428g=4.28mg,
所以1kg食盐中:m(KIO3)=10×4.28mg=42.8mg,
其中m(I)=42.8mg×127214=25.4mg>20mg,
所以可判定该食盐合格,
故答案为:42.8;合格.
本题解析:
本题难度:一般
5、选择题 甲装置中所含的是物质的量之比为1:2的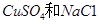 的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应)。试分析下列叙述中正确的是
的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应)。试分析下列叙述中正确的是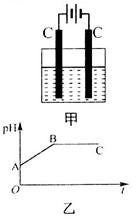
A.是该混合溶液中的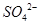 导致了A点溶液的pH值小于B点
导致了A点溶液的pH值小于B点
B.AB线段与BC线段在阴极上发生的反应是相同的即: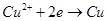
C.BC段阴极产物和阳极产物的体积之比为2:1
D.在整个电解的过程中会出现少量淡蓝色的Cu(OH)2沉淀
参考答案:C
本题解析:A、AB段阳极反应为:2Cl? - 2e? =Cl2↑,阴极反应为:Cu2+ +2e? =Cu,因为Cu2+浓度减小,水解产生的H+浓度减小,所以B点pH大于A点,错误;B、BC段阴极上反应为:2H+ +2e? =H2↑,与AB段阴极反应不同,错误;C、BC段溶液的溶质为Na2SO4,电解时水被电解,阴极产物为H2,阳极产物为O2,体积之比为2:1,正确;D、电解时溶液的pH≤7,不会出现Cu(OH)2沉淀,错误。
本题难度:一般